-
国务院推行新冠抗原检测试行方案 千亿市场迎爆发
产业研究院 / 2022-03-13 18:41 发布
新冠病毒的检测方法主要分为两种:一种是基于分子层面的核酸检测;一种是基于免疫学原理的检测,主要是抗原检测和抗体检测。
针对新冠病毒的防疫检测政策,欧美普遍采取抗原快速自测,而我国主要采取的核酸检测,区别就是抗原自测的操作简单,可以居家自行检测。而核酸检测的操作复杂,必须经由医疗专业人士,不仅增加了聚集感染风险,同时效率也非常低,大幅度增加了社会成本,也一直饱受诟病。
3月11日国务院印发通知,在核酸检测基础上,增加抗原检测作为补充,并组织制定了《新冠病毒抗原检测应用方案(试行)》。

目前相关抗原检测试剂盒厂商:万孚生物、九强生物、易瑞生物、东方生物、圣湘生物、亚辉龙、凯普生物、九安医疗、华大基因、诺唯赞。
300482 万孚生物
公司新品新型冠状病毒(2019-nCoV)抗原检测试剂盒(胶体金法)通过国家药监局应急审批,正式获得医疗器械注册证,成为首批获准上市的新冠病毒抗体现场快速检测试剂盒。
作为首批获准在国内上市销售的抗原试剂盒厂商,万孚生物无疑是抗原检测的市场总龙头。其重要程度可以对标前龙头九安医疗。
300942易瑞生物
1)新冠抗原检测原料药龙头
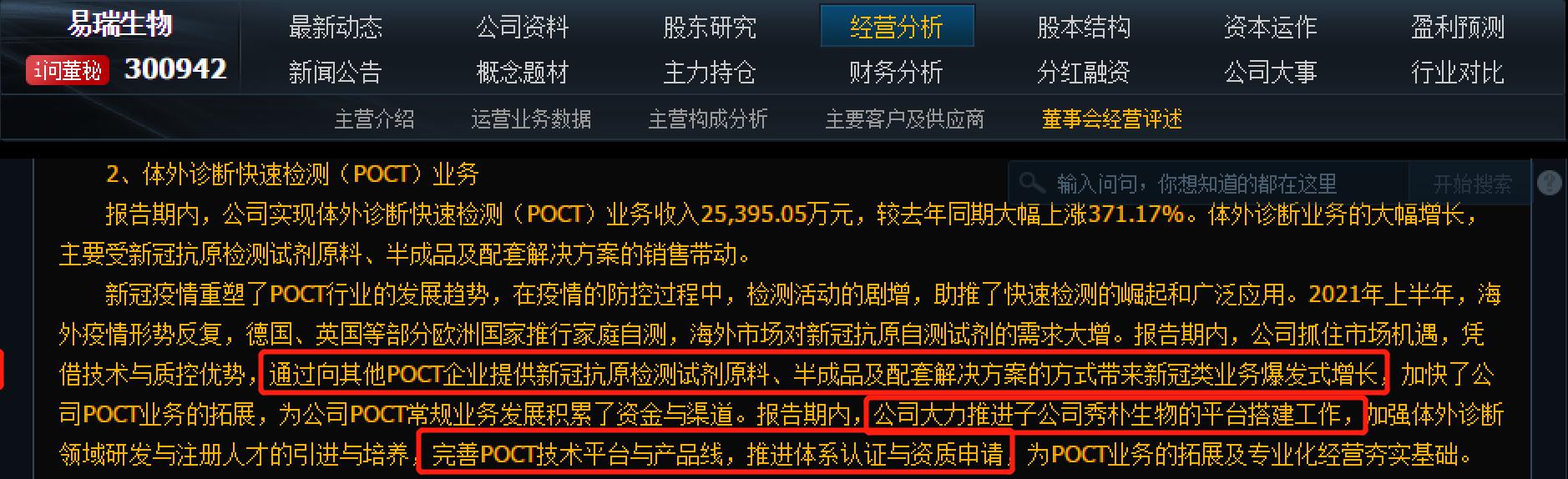
公司通过向其他POCT企业提供新冠抗原检测原料,半成品及配套解决方案,实现新冠业务爆发式增长。
公司经过多年研发积累,已成功研制出多种多样化检测物质的抗原抗体,其中有120余种自制抗原、140余种自制抗体已经批量用于生产,基本实现了主要产品所需抗原抗体自主生产,核心抗原抗体全部自产的良好局面,并且处于不断更新、优化之中,这使得我们具有的竞争优势有:1、保证产品质量的稳定性2、降低生产成本3、面对新的市场需求具有先发优势。
如果抗原检测取代核酸检测成为新冠检测主流,势必导致所有的检测厂商都会大幅度增加对抗原试剂原料的需求,原料采购价格和数量也会成倍的爆发!
2)PHASE SCIENTIFIC相达生物的合作伙伴及供应商

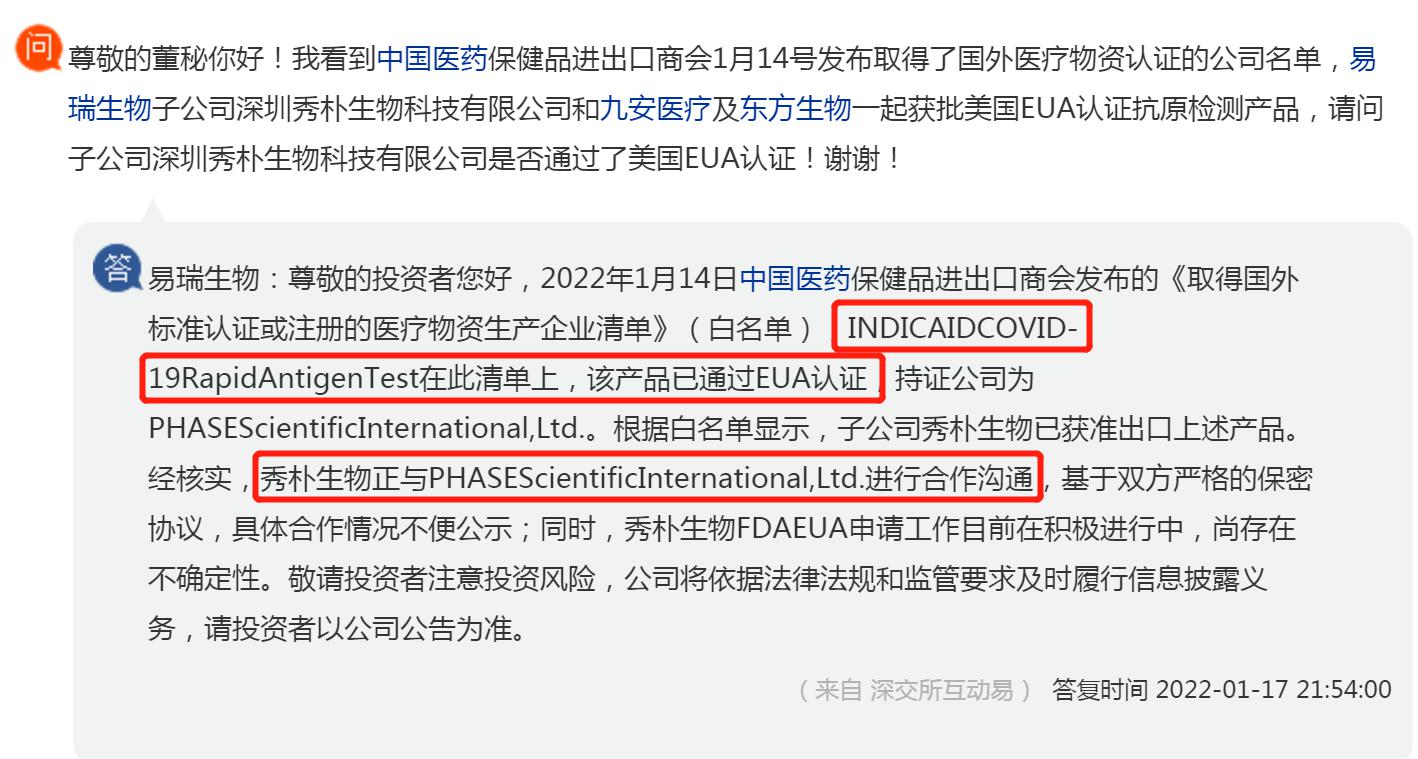
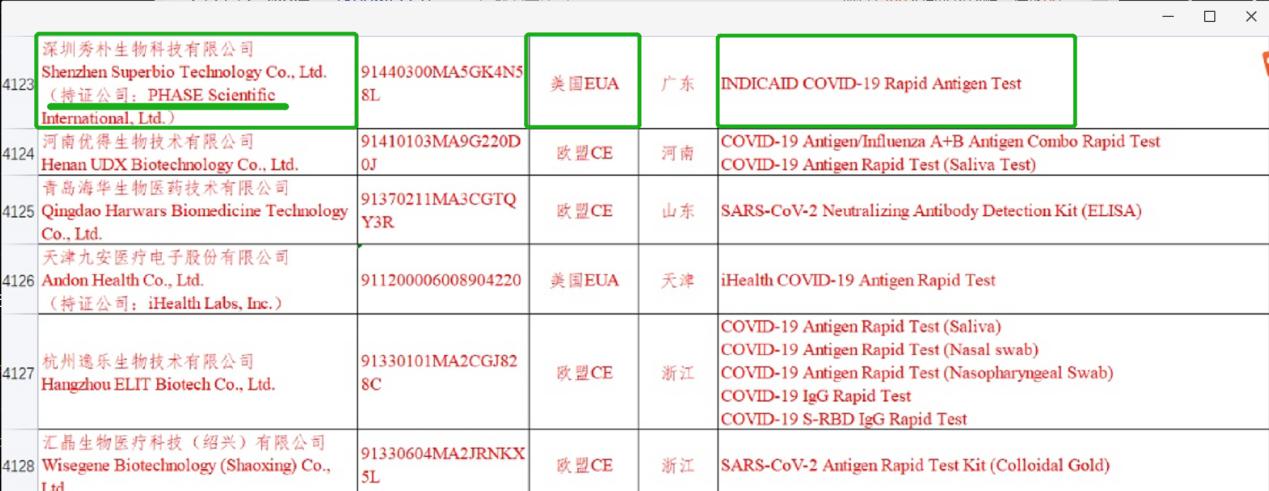
另据2022年1月14日中国医药保健品进出口商会发布的《取得国外标准认证或注册的医疗物资生产企业清单》,INDICAID COVID-19 Rapid Antigen Test(即“INDICAID妥析”试剂盒)在此清单上,该产品已通过美国EUA认证,持证公司为PHASE Scientific International, Ltd.(即相达生物)。这代表“INDICAID妥析”试剂盒进入国家商务部出口白名单,产品获准出口。同时据白名单显示,易瑞生物(300942.SZ)子公司秀朴生物也已获准出口该产品。
易瑞生物证券部人士回复《科创板日报》记者称,秀朴生物与PHASE Scientific是合作关系,并非为其代工,具体合作情况目前不便披露,后续会发公告。同时,秀朴生物美国FDA EUA申请工作目前在积极进行中,尚存在不确定性。
300406 九强生物
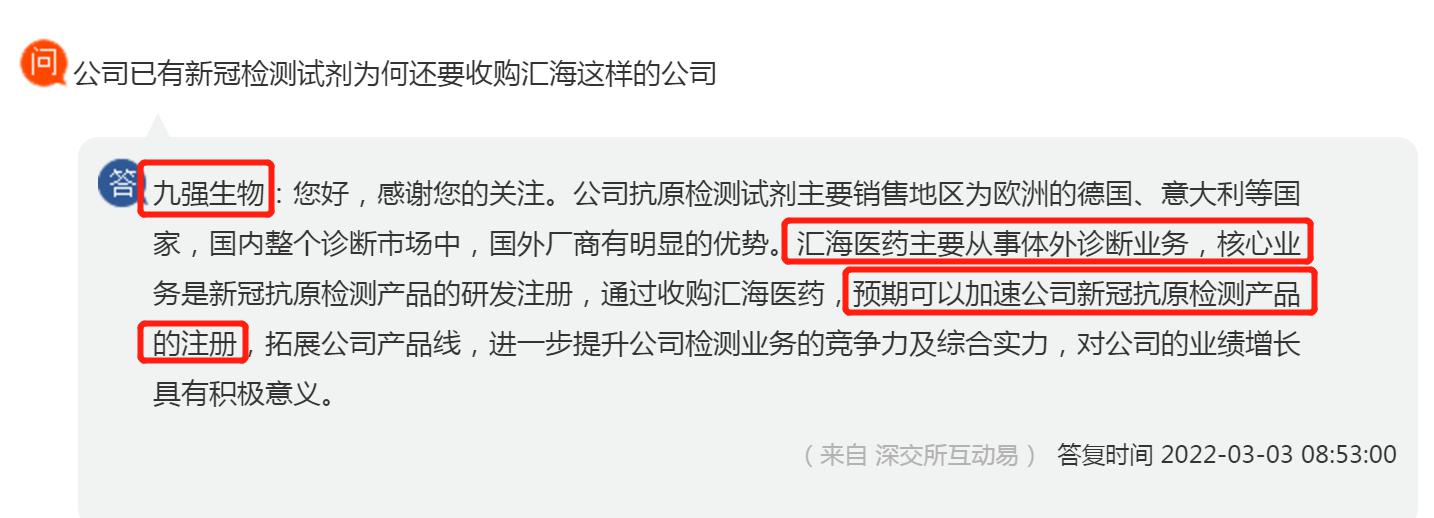
1)收购武汉汇海医药+申请第三类医疗器械注册,提前布局国内新冠自检市场
目标公司主要从事体外诊断业务,核心业务是新冠抗原检测产品的研发注 册。基于目标公司在新冠抗原检测领域的领先性及专业性,本次收购可以加速公 司新冠抗原检测产品的注册,拓展公司产品线,进一步提升公司检测业务的竞争 7 力及综合实力,对公司的业绩增长具有积极意义。
2)抗原检测获CE认证

公司已经在总抗取得了CE认证,医用版的抗原卡取得了CE认证,自测版的产品已进入审批流程。公司的新型冠状病毒抗原检测试剂盒可以检测奥密克戎新型冠状病毒突变毒株。公司的新冠检测试剂产品在意大利等国已有销售,海外销售前景十分乐观。

水晶球APP
高手云集的股票社区
X




 公安备案号 51010802001128号
公安备案号 51010802001128号