-
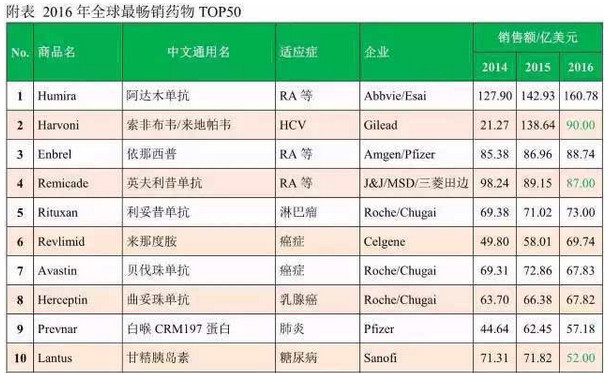
2017版医保目录解析(上)
价值at风险 / 2017-03-21 15:49 发布
注:作者为星瀚投资特邀医药研究员洪忠,本文借鉴不少券商研报(国元证券、中信证券、天风证券、东方证券)。本文不讨论估值和买卖点,仅对基本面作出梳理(有些A股特别是次新股公司估值高的吓人,显然不适合买入)。本文为上篇,介绍了部分企业,至于下篇,不知道什么时候会出,可能随时跳票。
2月23日,历时8年的新版医保目录终于尘埃落定,这是医药界的大事。各媒体、券商也第一时间从各方面解读了新版目录,增补内容都有详细列表,这里简单说说我们对医保目录的理解。
医保目录像考试大纲,规定了“范围”,圈定了“考点”,医保目录更像一张“文凭”、“敲门砖”,新进入医保目录的药品无疑给后续增长打开了想象空间,但并不是进入医保目录就如获珍宝,数数看哪家进入医保目录的品种数量多,而是要看品种的市场空间有多大,品种占有的市场率,品种的临床应用价值。而且产品的业绩释放需要一个过程,要看省级医保目录增补和支付标准制定、医院招标、医生开药,药企销售渠道的铺开。所以对医保目录需要客观的看待,具体的公司具体的品种具体分析。
医保目录调整中值得关注的点:
1. 中成药比预期的调入力度要大,虽然市场上普遍担心的中药临床路径不清晰而被限制使用,但显然国家重视中医药产业发展的大逻辑大趋势没有变,一些独家、市场空间比较大的品种值得关注。
2. 虽然重点支持了儿童药,新增91个品种,但从投资的角度总体来说,儿童用药由于特殊性难以产生很大品种,国家更多的是鼓励和关怀覆盖。
3. 本次目录调整有多个国产一类新药成功进入医保目录,包括贝达的埃克替尼、南京圣和的左奥硝唑、广州南新的帕拉米韦、恒瑞的艾瑞昔布、先声的艾拉莫德以及石药的丁苯酞等。可以发现,2008年至2016年上半年我国批准的创新化药和生物制品中,绝大部分都被纳入了2017年版药品目录范围或谈判药品范围,国家鼓励新药自主创新的氛围日益浓厚,虽然部分创新药上市后销量不佳也是事实,但随着产业升级、越来越多的资本投入到创新药的研发,国家开展创新药、临床价值高的高价药谈判制度,以后医保目录和谈判制结合,采取滚动式调整医保目录,将极大的促进创新药调整价格进入医保目录、放量增长,从而形成创新药企研发发展和医保控费的良性循环。
具体到公司新增加的品种,不同于市场过分聚焦入选品种数量这一最为明确的指标,我们认为应该从入选品种的临床价值、竞争格局和对公司业绩影响占比等多个维度进行综合分析。重点关注以下公司:易明医药、三生制药(港股)、恒瑞医药、广生堂、东化通宝、丽珠集团、华润双鹤、石药集团(港股)。
一、易明医药:新进医保品种占公司总销售额70%
易明医药是专注糖尿病、心脑血管病等老年慢性病品种的特色专科药企。目前公司业务包括自主生产和合作推广销售两大块。其中米格列醇片(糖尿病)、红金消结片(乳腺增生)、瓜蒌皮注射液(冠心病)进入本次新版医保目录。以上三款产品合计销售占比近70%,毛利占比更是高达75%。
公司新近医保品种基本状况:
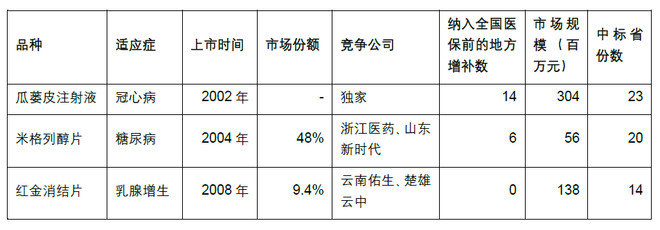
(1)米格列醇片
米格列醇片是一种新型降糖药,为公司拥有专利的国内首家仿制新药,主要适用于II 型糖尿病。米格列醇与同属于糖苷酶抑制剂类型的阿卡波糖、伏格列波糖相比,有如下优势:米格列醇对酶的抑制作用更强,范围更广,抑制效果更好;无肝损伤风险,服用更加安全,其他两种产品的代谢产物被吸收进体内,对肝脏造成损伤,需定期监测肝功能,而米格列醇片在体内不被代谢分解,无肝损伤;与阿卡波糖相比,米格列醇片的胃肠道不良反应发生率更低。此外,由于我国民众的饮食结构,高脂血症以高甘油三酯血症为主,米格列醇能有效降低甘油三酯水平,更加适合我国的糖尿病患者。其安全有效,副作用明显降低,已在多个国家被广泛使用,现已成为治疗 II 型糖尿病的首选药物,根据国外的数据分析有代替阿卡波糖之势。
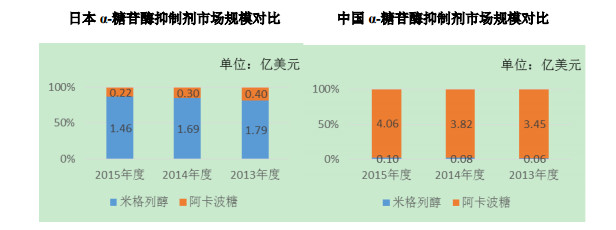
A、 米格列醇在糖苷酶抑制剂糖尿病用药市场的市场份额 2013 年至 2015 年,米格列醇在糖苷酶抑制剂糖尿病用药的市场份额稳步提 升,复合增长率已达 35.82%,复合增长率排名第一。具体如下:
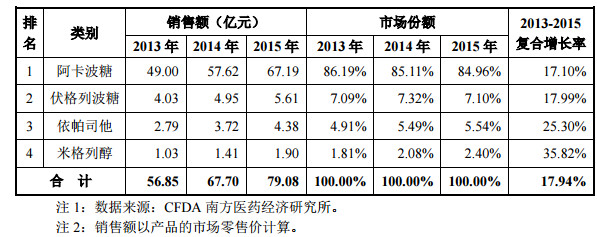
B、 易明医药在米格列醇制剂市场的市场份额:
在全国范围内,共有三家企业生产销售米格列醇片,分别为维奥制药(易明子公司)、浙江医药股份有限公司新昌制药厂和山东新时代药业有限公司。具体数据如下:
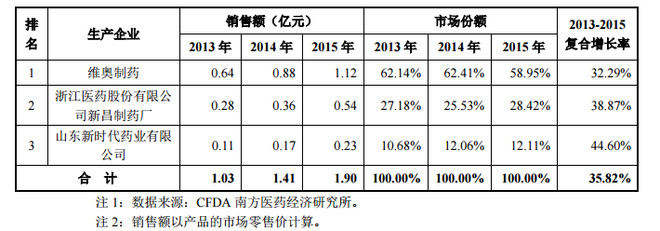
显而易见,易明医药的米格列醇片占据市场的绝大份额,而且一直保持30%左右的增速,米格列醇片之前进6省医保目录,这次进入全国医保目录,市场空间进一步增大,如果国内市场也随着国外市场阿卡波糖逐渐被米格列醇片代替之势,那米格列醇片的增长空间将不可估量,后续值得重点关注。
(2)红金消结片
红金消结片源于彝族中药的经典方剂,产品主要适用于治疗气滞血瘀型乳腺增生,也可用 于子宫肌瘤、卵巢囊肿、痛经等妇科顽症,具有独特的疗效。
A、我国气滞血瘀型乳腺增生中成药主要品种市场份额 2013 至 2015 年,红金消结片在我国气滞血瘀型乳腺增生中成药的市场份额 逐年提升,复合增长率达 29.29%,排名第一。具体如下:
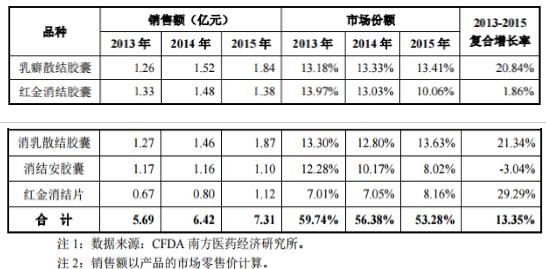
B、 易明医药在气滞血瘀型乳腺增生中成药市场的市场份额:
2013 年至 2015 年,我国气滞血瘀型乳腺增生中成药市场销售额排名前五位 的企业分别是山东步长神州制药有限公司、陕西白鹿制药股份有限公司、云南佑 生药业有限责任公司、云南良方制药有限公司、维奥制药(易明子公司)。其中,维奥制药的市 场份额稳步提升,三年复合增长率排名第一,达到 34.01%。具体如下:
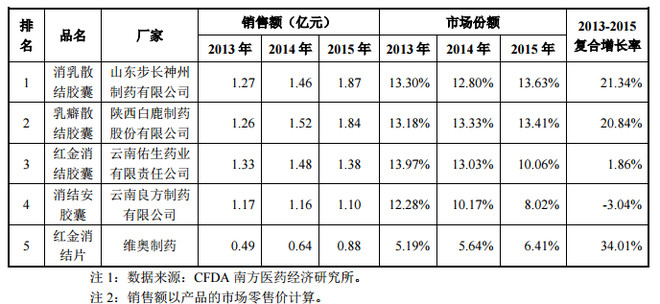
红金消结片销量过亿,且增长良好,进入医保后将继续为公司提升业绩。
(3)瓜蒌皮注射液
公司与第一生化合作的瓜蒌皮注射液,为全国独家品种,治疗心脑血管疾病的中成药,是目前国内唯一的冠心病痰浊阻络证中药注射剂,已有 15 个省区将其列为医保乙类品种,这次进入全国医保目录。从合作上看,公司负责瓜蒌皮原材料的独家供应,上海第一生化负责生产,上海医药另一只公司负责上海、浙江、湖南、青海和西藏的销售,而公司则负责除以上区域外的中国境内独家销售。
2013 年至 2015 年,瓜蒌皮注射液在我国心脑血管疾病中成药注射剂的市场 销售额稳步提升,三年复合增长率为 17.95%,高于销售额排名前五的注射液品种,具体如下:
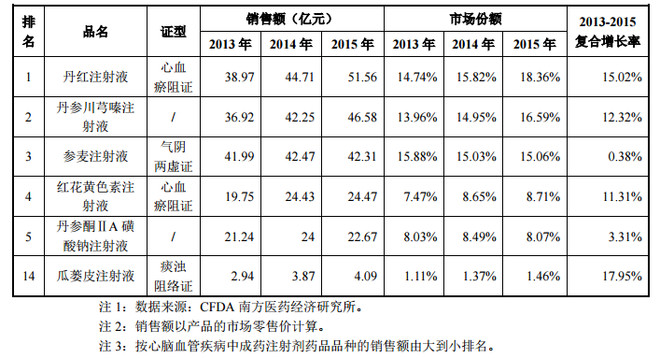
由于近几年中药注射剂的不良反应已经成为行业诟病其的依据,纷纷被叫停并纳入监管,这次医保目录调整,中药注射剂是被限制的一类,瓜蒌皮注射液也是限用在二级及以上医疗机构并有冠心病、心绞痛明确诊断的患者。但瓜蒌皮注射液是这次被调入医保目录三个中药注射剂品种其中之一,可见它在治疗冠心病痰浊阻络证的疗效和独特性,后续放量增长可期。
公司主要收入及利润来源于六种药品。情况如下:
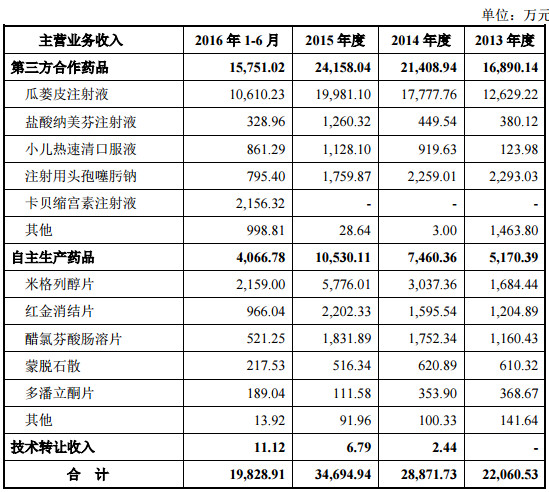
作为刚刚上市的次新股,估值自然是没法看了,并且作为一家位于西藏的医药公司,公司并无太高的技术含量,产品线虽有增速不错的小品种,但亦有中药注射剂这种高危品种,同时公司只有1/3的收入是来自于自主产品,其他均为合作和经销,研发投入非常低(研发投入1.7%)。最后,公司募投项目打算大力发展藏药,这让我对其未来的发展更不看好。财务质量上,公司虽然业绩增速不错,但应收账款大幅增长,为了上市而冲业绩迹象明显。
二、三生制药 :两大重磅品种特比澳(TPO)和益赛普双双入选
(1) 特比澳
特比澳(TPIAO)是三生制药的专利产品,国家一类新药,自2006年推出后一直是世界上唯一的商业化生成素产品,也是中国唯一获批的重组人血小板生成素产品。它的两个主要适应症是为化疗引起的血小板减少症(CIT)和免疫性血小板减少症(ITP)。重组人血小板生成素产品为二线治疗名单的首选推荐,并推荐于部分急救情况下用作促进血小板生成的药物,2015年特比澳在血小板减少症治疗用药市场中占据了41%的份额。2016年Q2,特比澳销售额约人民币4.05亿,比增37.4% (占公司收入31%)
潜在的竞品是安进公司研发生产罗米司亭和葛兰素史克研发生产的艾曲波帕。目前有两家国内企业按照生物仿制药申报:齐鲁制药(2013年11月)、山东泉港药业(2014年12月),总体来讲,特比澳的竞争根据是相对较好的。
目前,特比澳的大部分销售来自公司销售团队所覆盖约12%的医院,还有比较大的扩容空间,同时正计划于美国、印度及墨西哥进行特比澳临床试验。这次医保目录调整由工伤保险扩大至限实体瘤化后所致的严重血小板减少症和特发性。可以说报销的范围扩大了很多,将大大促进特比澳的放量增长。
(2)益赛普
益赛普是三生国健于2005年推出的肿瘤坏死因子TNFа抑制剂产品,是第一个在内地上市的依那西普产品,主要用于治疗类风湿关节炎,也可用于治疗强直性脊柱炎和银屑病。2016年Q2益赛普实际销售额为4.46亿人民币,比增16.5%(占比公司收入23%)。占64%的内地市场份额,由于益赛普是国内第一个被市场接受的国产依那西普的生物类似药,且价格比进口药物优势明显,已形成较为稳定的市场格局,而作为治疗风湿性关节炎或强直性脊柱炎的产品,病人需要长期注射,具有稳定的需求。目前,肿瘤坏死因子仅有海正(安百诺2015年上市)、三生(益赛普2005年上市)和上海医药子公司上海赛金(强克2011年上市)3家公司获批生产,国外竞争品阿达木、类克、恩利因为价格昂贵一直没打开国内市场,竞争格局相对良好。
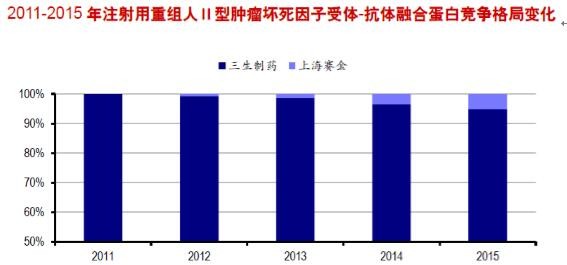
虽然此次调整进入全国医保目录乙类,但此前已经进入7个省市的增补医保目录,而且做了诸多限制:限诊断明确的类风湿关节炎经传统DMARDs治疗3-6个月疾病活动度下降低于50%者;诊断明确的强直性脊柱炎(不含放射学前期中轴性脊柱关节炎)NSAIDs充分治疗3个月疾病活动度下降低于50%者;并需风湿病专科医师处方。但鉴于中国单克隆市场的渗透率较全球市场为低(国内1000多万风湿病患者,只有7%~8%的患者会使用生物制剂,而国外常规可达到30%。所以后续的市场增长潜力还很大。)相信益赛普于中国仍处于产品生命周期的早期阶段,一旦符合医保要求的患者使用注射肿瘤坏死因子抑制剂是大概率事件。
总的来说,三生制药核心品种就三个,这次两大重磅品种特比澳(TPO)和益赛普双双入选医保目录,受益是最明显的,医保目录公布当天三生制药(港股)上涨20%也是很好的印证。公司在香港上市,同时因中信国健收购费用、产品撤回、研发支出大等因素导致利润承压,估值偏低。
三、恒瑞医药:国内创新药企龙头,4大品种入选,在研3大品种入选。
恒瑞此次入选医保目录的品种有右美托咪啶、非布司他、达托霉素、艾瑞昔布,同时在申报的帕立骨化醇、磺达肝葵钠、聚乙二醇重组人粒细胞集落刺激因子入选。另外阿帕替尼有较大可能通过谈判进入目录。据此,我们重点分析非布司他、右美托咪啶、艾瑞昔布和阿帕替尼。
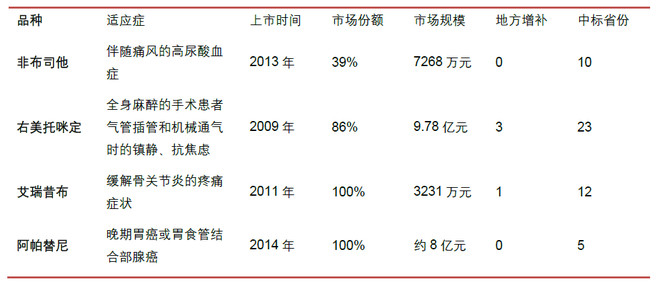
(1)非布司他
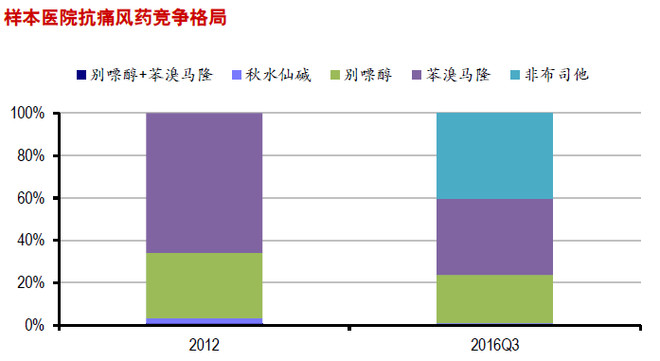
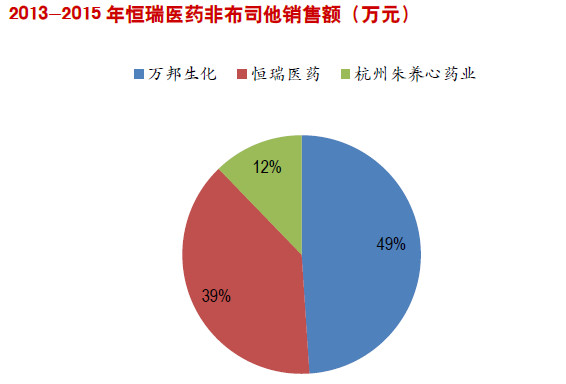
由日本武田药业研发的一种新型非嘌呤类选择性黄嘌呤氧化酶抑制剂,2009年经FDA批准在美国上市,用于长期治疗伴随痛风的高尿酸血症。与目前治疗痛风的标准药物别嘌呤醇相比,非布司他具有更高的选择性和更强的活性。目前,痛风的治疗方法主要有两种,分别是促进尿酸排泄和抑制尿酸合成。临床治疗主要以秋水仙碱、类固醇抗炎药、激素、促进尿酸排泄药(如苯溴马隆)和抑制尿酸合成药(别嘌呤醇)为主,这些药物耐受性差、副作用多,在临床应用上有较大的瓶颈。 据保守估计,我国高尿酸血症的患者人数达到了1.2亿人,其中痛风患者超过了7500万人,并且维持约1%的年增长率,存在较大的治疗需求。从样本医院销售情况来看,抗痛风药市场规模保持了较快增长,11-15年CAGR达到34.88%,16年前三季度同比增速高达55%。
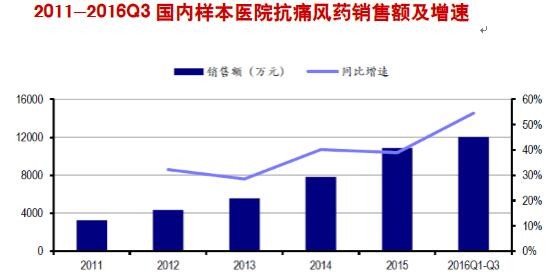
非布司他上市后销售规模迅速增长,成为临床抗痛风药的最大品种。非布司他于13年上市,15年实现销售额7268万元。根据样本医院数据,截至16年前三季度,非布司他市占率已经达到40%,超过苯溴马隆、别嘌醇和秋水仙碱。从竞争格局上看,非布司他国内仅有3家企业获批,恒瑞医药市占率居第二位。据样本医院数据显示,16年前三季度恒瑞医药市占率达到39%。非布司他调入国家医保目录将会更快地释放临床需求,相关公司将明显受益于该品种销售放量。
(2)右美托咪啶
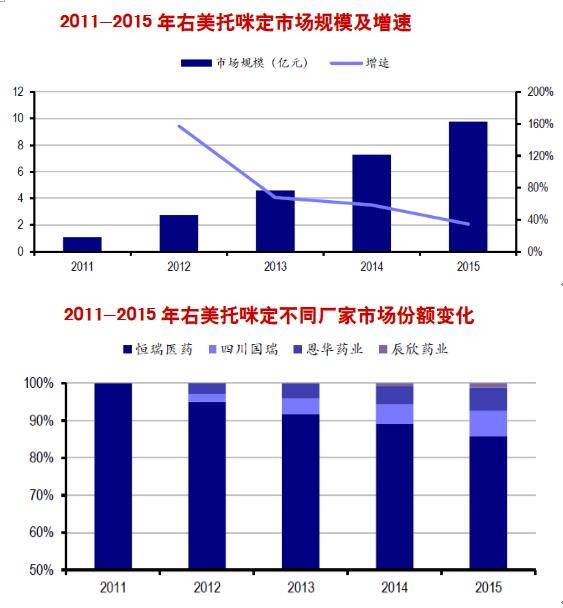
右美托咪啶是高选择性α2 肾上腺素能受体激动剂,具有中枢性抗交感和产生近似自然睡眠的镇静作用;同时具有一定的镇痛、利尿和抗焦虑作用。右美托咪啶临床中主要用于全身麻醉的手术患者气管插管和机械通气时的镇静、抗焦虑,可减少麻醉药的用量、降低麻醉和手术引起的交感兴奋效应,提高血流动力学的稳定性。 目前,催眠镇静药在精神方法障碍类用药中所占份额较大,仅次于抗抑郁症用药和抗精神病药。据估算,2016年催眠镇静药占精神障碍用药整体规模大约为21%。催眠镇静用药市场规模近年保持快速增长。PDB数据显示,11-15年市场规模年均复合增长率高达34.69%;16年前三季度同比增速达到31.47%,较2015年有所提升。
右美托咪定临床应用有以下特点:1)可即时唤醒;2)对呼吸抑制作用弱;3)唯一具有镇痛作用的镇静药,可减少镇痛药物的用量,提高安全性。作为传统品种咪达唑仑的升级版,右美托咪定安全性更高、副作用更小,临床需求较为强烈。右美托咪定09年首仿上市,至15年销售额已接近10亿元;11-15年销售年均复合增速达到60%。恒瑞是国内右美市场的主导者,且近期维持了15%-20%的增速。由于右美价格较高(2mg规格中标价在160-180元/支),此次纳入医保目录将有助于右美解决支付限制,各厂家将直接受益,长期看恒瑞的右美销售规模有望达到20亿元级别。
(3)艾瑞昔布
是新一代非甾体抗炎类创新药,属于 COX-2 酶抑制剂,主要用于缓解骨关节炎的疼痛症状。恒瑞医药于 1999 年开启该品种的临床前研究,是公司第一个获批上市的国家一类新药。相比传统药物而言,艾瑞昔布安全性更高、依从性更好,是关节疼痛、骨关节炎的一线治疗药物。
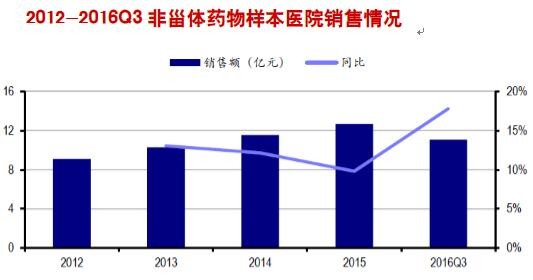
非甾体抗炎药市场规模增长较快,整体空间已达50亿元。非甾体抗炎药在临床上广泛用于骨关节炎、类风湿性关节炎、多种发热和各种疼痛症状的缓解。我国类风湿关节炎患者约400~500万人,骨关节炎患者高达1.2亿,存在较强的临床需求。根据样本医院数据,非甾体药物12-15年CAGR达到11.62%,15年销售额达到12.67亿元。
可媲美原研的重磅品种。1999 年第一种选择性COX-2 抑制剂辉瑞的塞来昔布经FDA 批准上市,用于治疗风湿性关节炎和骨关节炎引起的疼痛。艾瑞昔布缓解骨关节炎患者疼痛症状的效果和胃肠道安全性方面与塞来昔布相当,心血管、肾功能安全性更优,是理想的昔布类抗炎药。 近年,塞来昔布销售规模已达8亿元左右。艾瑞昔布上市初期销售推进并不理想,在进入江苏省医保后单省销售即可达到之前全国销售额,可见医保弹性巨大。预计进入全国医保后艾瑞昔布销售规模可迅速破亿。
(4)阿帕替尼
甲磺酸阿帕替尼是由恒瑞医药研发的酪氨酸激酶受体抑制剂类的靶向小分子药物,主要通过高度选择性地抑制血管内皮生长因子受体酪氨酸激酶的活性,阻断血管内皮生长因子与其受体结合后的信号转导通路,从而强效抑制肿瘤血管生成,发挥抗肿瘤作用。临床用于晚期胃癌或胃食管结合部腺癌三线及三线以上治疗,于2014 年10 月经CFDA 批准作为国家1.1 类新药上市。
临床价值较高,安全性有效性得到验证。阿帕替尼III 期研究结果不但证实了阿帕替尼的客观有效和安全性好,同时还证明了它能够为晚期胃癌患者带来明显的生存获益。据专家共识,临床上阿帕替尼延长二线治疗失败的晚期胃癌患者生存期和无进展生存期效果显著,是晚期胃癌标准化疗失败后疗效最好的单药。
我国胃癌发病死亡率高,药物需求空间大。据全国肿瘤登记中心统计,2015年我国胃癌年新发病例超过42 万例,发病率和死亡率分别为22.7/10万人和17.9/10万人,均位居各种癌症前列。由于胃癌早期症状不典型,普查不及时,目前在我国早期胃癌的诊断率不足10%,约有65%-70%的胃癌患者在就诊时已经达到中晚期,5年生存率仅为27.4%。
晚期胃癌的一线化疗药物为铂类和5-氟尿嘧啶,二线化疗药物为紫杉醇类和伊立替康,这些药物都是细胞毒性药物,且治疗效果并不理想,所以阿帕替尼虽然作为三线药物,仍然有较大的治疗需求。按照国内每年新增三线胃癌病人10万人,治疗意愿50%来估算,则阿帕替尼的潜在市场空间大约为30亿元。2015年,阿帕替尼销售额大约为2.6亿元;2016年上半年销售额约为4亿元,呈现出稳定增长态势。如果谈判成功,放量更加明显。
另外磺达肝葵钠和帕立骨化醇作为国内首仿(审批中)也均进入医保,磺达肝葵钠公司尚在审评,预计与华东医药审评进度接近。磺达肝葵钠是第一个靶向的抗Xa因子无血小板减少的副作用,临床应用药品无需监测的优良品种抗凝血药,是肝素系列抗凝血药物中最后的全合成产品。2015年样本医院销售约805万元,本土企业尚无获批。帕立骨化醇是一种合成的、选择性、第3代维生素D受体激活剂,用于预防和治疗与慢性肾病(现在指接受血液透析的慢性肾病患者)相关的继发性甲状旁腺功能亢进症。由于价格较高(1ml规格中标价约340元)、赫士瑞推广时间较短,目前国内市场规模不大。随着进入医保解决支付问题,公司帕立骨化醇上市后将与原研共同开拓市场,预计长期销售规模可达2-3亿元。
毫无疑问,公司核心品种增长稳健,在肿瘤、糖尿病、麻醉、造影等均衡布局,制剂出口已打开窗口,此次的4个重大品种进入医保目录更加能够保持稳健的增长。这里感慨一下,曾经的恒瑞主要营收也只是靠多西他赛等抗肿瘤药,和国内其他制药企业并没有拉开太大差距,但公司一直沉下心来,埋头走研发创新之路,现在已形成了良好的产品梯队,生物制药也得到了很好的布局,进入创新之路的收获期。现在公司的估值有点偏高。
四、广生堂:替诺福韦如期纳入,有望为公司带来重要业绩增量
作为2015年谈判品种,替诺福韦二吡呋酯如期纳入医保乙类目录(限有活动性乙型肝炎的明确诊断及检验证据或母婴乙肝传播阻断)。 替诺福韦二吡呋酯是核苷类抗病毒药物,主要用于治疗慢性乙肝和艾滋病。目前,国内尚未有替诺福韦乙肝适应症的仿制药。
国内潜在首仿,市场空间大。2016年7月21日,CFDA发布《“首仿”品种实行优先审评评定的基本原则》,并公布22个优先审评的品种,广生堂的替诺福韦酯胶囊(乙肝适应症)即在名单中。目前,公司的替诺福韦酯胶囊(乙肝适应症)已经完成补充资料任务的所有内容(包括临床和药学评审),仅剩三合一现场检查项目。在目前申报替诺福韦仿制药的企业中,广生堂替诺福韦进度最快,我们预计公司的替诺福韦酯(乙肝适应症)将于今年3月左右份获批,大概成为我国第一个替诺福韦乙肝适应症的仿制药。
目前我国约有乙肝携带者1.2亿人,其中慢性乙肝患者约2000万人。从理论上讲,此2000万名慢性乙肝患者均需要长期服药,市场规模广阔。然而,目前乙肝患者实际用药的人数只有200万人左右,渗透率不足10%,主要原因还是乙肝治疗费用高,且医保报销比例不足。2016年6月,卫计委药品谈判结果公布,其中替诺福韦酯的月均费用从1470元/月降低到490元/月;同时,此次医保目录调整,替诺福韦纳入医保乙类报销目录,这使患者的治疗压力大大降低,这也给替诺福韦用量打开了空间。
替诺福韦与恩替卡韦的竞争并不激烈,二者有望长期共存,共同扩大我国乙肝用药市场。我们认为:替诺福韦对恩替卡韦的替代更多表现在市场份额上的替代,但替诺福韦的用药人群,并非完全来自恩替卡韦目前用药人群的替换(即恩替卡韦的用药人群,转而服用替诺福韦)。使用恩替卡韦向替诺福韦转化的患者主要是交叉耐药的患者(即原来使用拉米夫定、阿德福韦酯耐药,随后使用恩替卡韦的患者),这部分患者约占恩替卡韦总用药人数的四分之一。 而替诺福韦对恩替卡韦市场份额的替代,则更多体现在首次用药的患者。我们认为,未来首次用药的患者,直接选择替诺福韦的比例将多于恩替卡韦(我们大致估计,首次用药人群,选择替诺福韦人数:选择恩替卡韦的人数约为6:4),诺福韦的市场份额从而逐渐扩大。 换句话说,与其说是替诺福韦与恩替卡韦在分蛋糕,不如说二者在共同做蛋糕。
我国乙肝市场的实际渗透率不足10%,目前远未达天花板,其核心问题在于经济负担和疗效(包括耐药管理)。替诺福韦的降价与进入医保,恩替卡韦的中标价降低,为患者提供了更实惠、效果更好的治疗方案,将促进乙肝用药人群的快速扩大。在这种情况下,我们认为,替诺福韦与恩替卡韦虽然存在一定的竞争,但随着我国乙肝用药人群的增加,我国乙肝市场规模进一步扩大,替诺福韦和恩替卡韦的用药市场规模都将扩大。
我们以国外的实际情况为例,在美国,虽然替诺福韦的耐药管理优于恩替卡韦,适用人群也更广,但恩替卡韦副作用较替诺福韦稍小,所以在国外部分医生倾向于推荐病程较轻的病人使用恩替卡韦,恩替卡韦在美国依然占据30%左右的市场份额。 “韦瑞德”和“博路定”作为原研品种,分别为替诺福韦和恩替卡韦的代表药物,从全球销售额上看,2015年,“韦瑞德”全球销售额为11.08亿美元,“博路定”全球销售额为13.12美元,二者差别并不算大,但“韦瑞德”自从2008年获FDA批准用于治疗乙肝之后(此前只获批治疗HIV),销量不断上升,而“博路定”略有下降,预计在不远的将来“韦瑞德”销售金额将超过“博路定”,但二者会长期并存,同为当前阶段乙肝治疗的主流用药。未来,我们认为替诺福韦和恩替卡韦也会成为我国乙肝用药的两大主力,长期并存。
总之,乙肝治疗市场空间大,竞争也大,正大天晴、成都倍特、齐鲁制药的批文也都在评审中,加上恩替卡韦竞争,广生堂需要拔得先机。公司2016年业绩因受恩甘定产品价格下降和研发费用增加(增加丙肝艾滋品种研发)影响,同比仅增长1.28%,净利润同比减少35.71%,但其实其核心品种恩甘定销量还是增长,销售收入还是同比增长20.17%,加上替诺福韦纳入医保,生产批文下来,2017年或许能扭转颓势。
五、通化东宝:二代胰岛素调为甲类,三类使用明确受限
通化东宝此次二代胰岛素由乙类调整为甲类,三代胰岛素适用范围被赋予明确限制。下图为通化东宝二代胰岛素销售金额和二代胰岛素市场竞争格局:
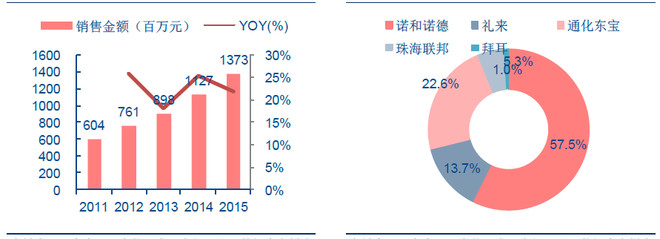
二代胰岛素2013年已进入基药,此次调为甲类是预期内事件。在国外公司逐渐放弃二代胰岛素开始转战第三代胰岛素市场的情况下,东化通宝却瞄准中国广大县级农村,细耕二代胰岛素市场,我们觉得这是符合国情的。需要特别指出的是,公司独家的40R预混胰岛素此次亦明确被列入医保甲类,将大大有助于公司推广。特别是部分竞争对手以价格优势抢占部分区域市场后,公司采取的主要策略是以40R补标进入,此次纳入医保甲类意义重大。
同时胰岛素类似物的适用范围被明确为在二代胰岛素难以控制的患者,这一规定相对于09版的限反复发作低血糖或有重度并发症的老年患者,更为明确和易于界定。我们预计此次医保目录出台后将有助于二代胰岛素推广和公司40R放量,将小幅抬升公司销售增速。
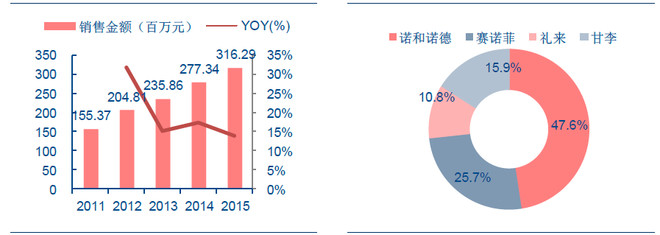
总体来看,东化通宝短期估值有点偏高,不建议介入。但长期看考虑到国内糖尿病市场巨大,渗透率较低,通化东宝能在第三代胰岛素和降糖药DPP4抑制剂(现在受益的都是国外公司,国内恒瑞、齐鲁、正大天晴均在仿制中)方面推出新的品种,仍能保持不错的增速,市值上千亿也可能不是神话。
六、丽珠集团:艾普拉唑入选众望所归,注射剂型即将获批
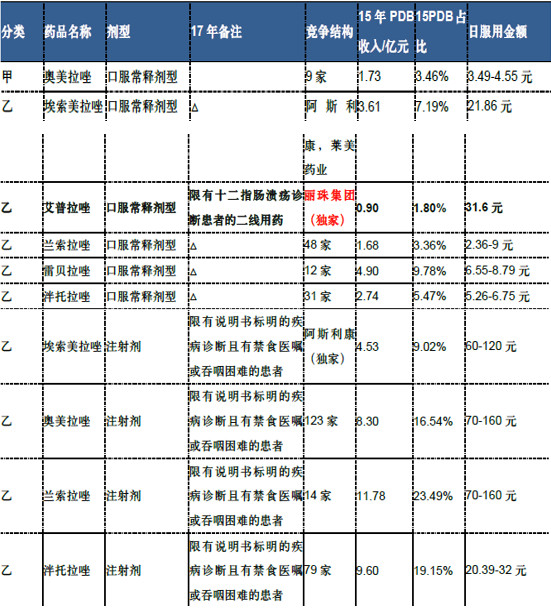
质子泵抑制剂是目前治疗消化性溃疡最先进的一类药物,市占率接近90%处于治疗绝对统治地位,为近十几年来临床应用广泛、疗效最好的药物。此次医保目录调整,丽珠集团的艾普拉唑是唯一新增的质子泵抑制剂类药物。目前国内上市的拉唑类药物包括奥美拉唑、兰索拉唑、泮托拉哇、雷贝拉唑、埃索美拉唑和艾普拉唑,艾普拉唑作为新一代PPI,药物性状可与埃索美拉唑媲美,具备良好的治疗作用。
艾普拉唑是丽珠集团独家开发的第二代质子泵抑制剂(PPI),是国家I类新药, 2008年上市,在十二指肠溃疡治疗方面独具优势,其显著改善了同类药物抑酸时间短、个体差异大、药物相互作用多的缺陷,通过创造性地集成构效设计、胃酸pH监测和基因分型技术,运用原料药氧化和结晶关键技术等,共申请发明专利37项,获美国、欧洲等23项专利授权。2015年在未进入国家医保情况下实现近2亿销售,2016年销量预计约3亿元左右,近几年均保持60%以上的增速,但相比较于全国近150亿元的拉唑类药物市场,艾普拉唑的规模依然较小,2015年占比仅不足2%。现进入17版医保目录后期有望占据较大市场份额,为潜力重磅品种。 除片剂剂型进入医保的重大利好外,丽珠集团申报的艾普拉唑注射剂剂型已进入上市申请阶段,预计今年获批。根据样本医院数据显示,质子泵抑制剂领域的注射剂市场占有率大于口服常释剂型,艾普拉唑注射剂有望获得更大市场空间。
七、石药集团:长效重组人粒细胞集落刺激因子的王者之师
此次医保目录调整,石药集团纳入的品种有重组人粒细胞集落刺激因子(长效)、丁苯酞注射液和恩必普。
(1) 重组人粒细胞集落刺激因子(G-CSF)
常用于肿瘤放化疗后导致的白细胞减少,是目前常用的“升白”药物。除此之外,G-CSF还用于骨髓移植中造血干细胞的动员和移植后骨髓造血功能的重建等原因引起的中性粒细胞减少症状。G-CSF是国内外临床指南首推的放化疗相关的中性粒细胞减少药物,可分为长效和短效两种类型。短效G-CSF在化疗周期内需要每日给药1-2次,而长效G-CSF主要是通过聚乙二醇化修饰实现了一个化疗周期中仅仅需要给药1次,方便性提升较大。
目前,从国内的情况看,G-CSF用药市场增速趋缓,但长效G-CSF占比迅速上升。根据样本医院数据,国内G-CSF市场规模大约为7亿元,估算以后整体销售规模约为30亿元。美国Amgen公司在1991年推出了全球首个重组人粒细胞集落刺激因子Neupogen,迅速被临床广泛接受。Neupogen近20年的销售额一直稳定在10亿美元以上。2002年,Amgen又推出了全球首个长效G-CSF药物Neulasta,截至2015年其全球销售额已高达47.15亿美元,并且在全球几乎垄断了长效G-CSF市场。
所以预计国内长效品种在医保推动下,有望促使产品快速放量,公司目前在国内长效G-CSF市场中占比最大(90%)。
(2) 丁苯酞注射液
主要用于急性缺血性脑卒中患者神经功能缺损的改善,是石药集团的重要品种。根据PDB数据,丁苯酞注射液在样本医院的销售额从2011年的687万元增长到2015年的1.73亿元
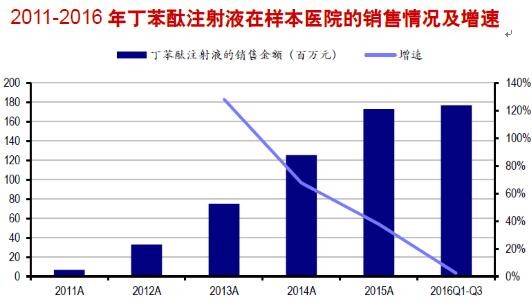
总的来说,石药产品线丰富,体量较大,此次医保目录对其影响并不大。
八、华润双鹤:匹伐他汀
据统计,2015年国内他汀类药物规模达到了151.4亿元左右,占有整个降血脂用药市场的80%,其中阿托伐他汀和瑞舒伐他汀规模较大,规模分别约为89.2、23.4亿元。匹伐他汀上市时间较晚(日本兴和的原研产品和华润双鹤的首仿产品均于2008年在国内上市),但凭借疗效明显,服用剂量小且目前唯一未见增加新发糖尿病(匹伐他汀与瑞舒伐他汀同为第三代他汀类药物),上市后迅速放量,2015年终端市场规模约6.7亿元,同比增长约111.0%。
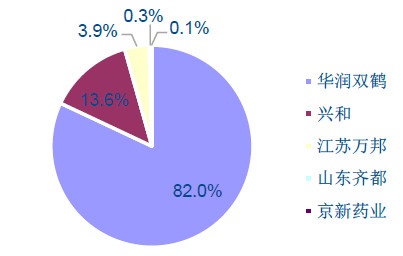
由于匹伐他汀过去未进入09年国家医保,较已进入国家医保的阿托伐他汀、瑞舒伐他汀市场规模较小。预计此次匹伐他汀被调入国家医保后,其市场空间将迅速打开,长期空间有望达到30亿元。公司2016年销量预计为2.6亿元,市场占有率约82.0%,进入医保后长期增长空间可期。
匹伐他汀2016年竞争格局:
九、本次目录保留彩蛋:
为了鼓励疗效确切的高价药品种,本次新版目录首创的新增45个品种的拟谈判目录,下一步有望通过谈判降价后再纳入目录范围,目前包括恒瑞医药的阿帕替尼、康弘药业的康柏西普、天士力的尿激酶原、信立泰的比伐卢定、绿叶制药的力扑素等品种都有望进入谈判,等具体目录出来再详细解读。
这次医保目录调整的重要性不言而喻,但从投资的角度来讲是多维性的,受制于标的公司的价格、体量。有些公司如易明医药、三生制药这次进入医保目录的产品占比公司总营收很大,自然受益是最明显的。有些公司虽然重磅品种这次进入医保,单此品种影响很大,但其公司总的体量很大,或者估值已高,对整个公司的影响又不一样。此次分析的重磅品种还需和公司总的估值等其他因素结合,形成综合的投资策略。
水晶球APP
高手云集的股票社区
X




 公安备案号 51010802001128号
公安备案号 51010802001128号