-
泰格医药,ROE、净利润率大幅提升创新高
江辉价值远航 / 2020-04-16 22:46 发布
今天泰格药业公布年报了,简单聊一下,周末再出详细的深度报告。
按惯例先看一下行业整体情况,今天增加了一个外资和内资的持仓哦!
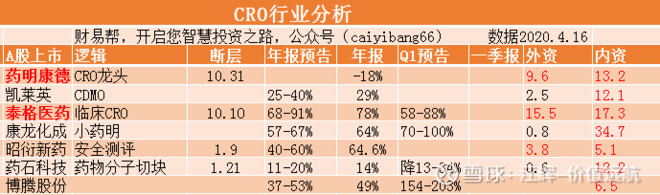
在看之前大家可以先看一下2月4日在发的文章--高成长的临床CRO龙头-泰格医药
一、财务数据:
营业收入280,330.93万元,较上年同期增长21.85%。归母公司净利润84,163.48万元,较上年同期增长78.24%。
新增合同金额为423,087.36万元,较上年同期增长27.90%。截至2019年12月31日,公司累计待执行合同金额为501,116.04万元,较上年同期增36.05%。
(1)临床试验技术服务业务本报告期稳步增长,实现主营业务收入134,667.22万元,较上年同期增长22.05%;临床试验相关服务及实验室服务本报告期稳步增长,实现主营业务收入144,648.18万元,较上年同期增长21.08%。
(2)报告期内,境内业务收入160,012.51万元,占比57.08%,较上年同期增长29.63%;境外业务收入120,318.42万元,占比42.92%,较上年同期增长12.84%。本报告期境内业务收入增长主要由于境内创新药临床试验业务占比增加所致。
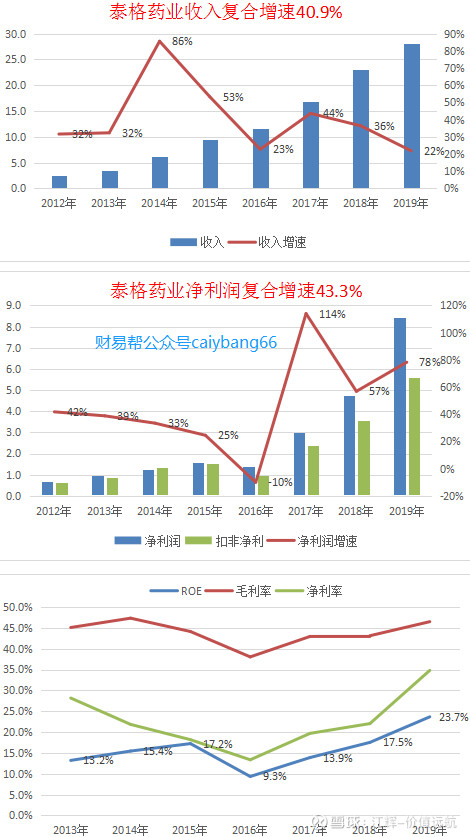
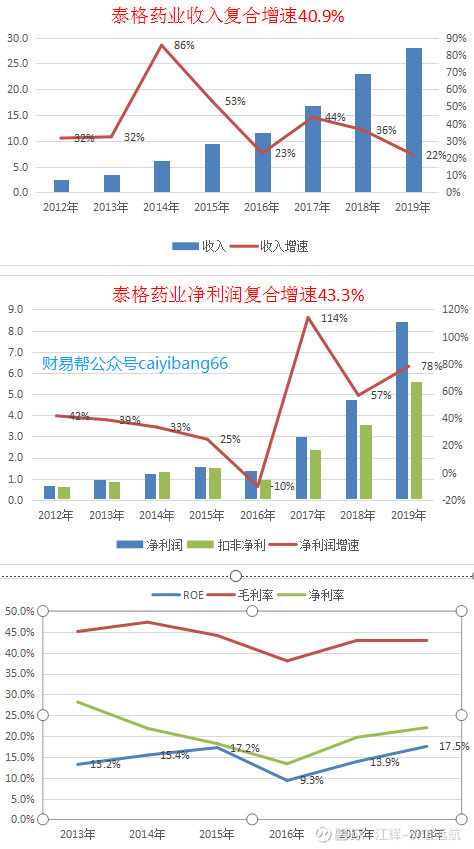
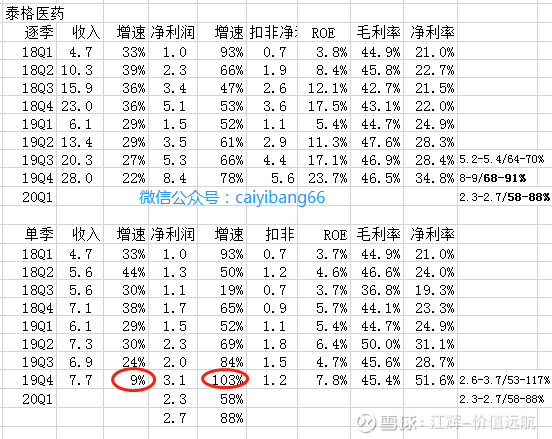
二、成绩
2019年度公司继续坚持“深耕中国,卓越全球”的发展战略,持续推动组织变革,加强集团化管理以适应公司发展,完善全球化布局,优化运营管理流程,推进组织能力和品牌文化建设,各个业务板块形成合力,全方位提升新药研发服务能力,业绩也保持了快速增长。
1、本年度,公司持续完善服务能力,深化全球布局
截至本报告披露日,公司已有123个国内服务网点(含中国香港、中国台湾),覆盖全国800多家药物临床试验机构,并在亚太、北美、欧洲等地区的10个国家设立海外子公司,广泛的服务网络能帮助客户迅速开展临床试验;通过战略性收购和自建,力求实现服务多元化,扩大全球业务服务能力。公司是创业板27只被纳入明晟公司(MSCI)中国指数的股票之一,是CRO行业首批入选的公司之一,公司的海外影响力持续增强。
2019年5月方达控股在香港联合交易所有限公司主板正式挂牌上市,方达控股提供贯穿整个药物发现和开发过程的一体化、科学驱动的研究、分析和开发服务,协助制药公司实现药物开发目标。方达控股在美国和中国均拥有业务,可以把握两个市场的增长机遇并受益于其中。
2019年公司成功在新加坡入组首例受试者,临床试验迎来新的里程碑。新加坡是东南亚的门户国家,具有世界一流的医疗服务体系、国际水平的临床研究者和经验丰富的研究团队。2019年7月30日,江苏晨泰医药科技有限公司开发的新一代口服小分子可逆性表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKI)—AZD3759的国际多中心II/III期临床研究成功完成在新加坡的首例入组和给药。该临床研究由公司助力开展,这也泰格医药在新加坡开展的首个国际多中心临床试验,以及在新加坡入组的首例受试者,未来公司也将由此向更多有潜力的东南亚国家提供研发服务。
2019年11月,泰格医药与Accerise株式会社共同宣布,双方将成立合资公司,提供在日本开展的国际多中心临床试验服务,以及为国内制药、医疗设备企业的全球开发提供支持服务。
2019年12月,公司自筹资金约1,774.33万美元购买了日本CRO领军企业EPSホールディングス株式会社(EPS控股有限公司,以下简称“EPS”)的140万股普通股,持股比例为3.06%。EPS是一家在日本东京证券交易所第一分部(主板市场)上市的公司,主要为制药公司、医疗器械厂家、新药研发公司、医疗机构、大学研究机构等众多客户提供各种高附加价值的解决方案,支持客户的产品开发。本次交易完成后,公司将与EPS建立长期合作关系,有利于公司进一步拓展亚太区业务。
公司持续改进、逐步优化质量管理体系,为最终达到临床试验全球最高质量标准的目标而时刻准备着。公司计划通过3至5年的建设,不仅在业务层面,还涉及各个职能部门层面,都能达到一个全球高的质量标准,使运营不断地持续优化,以更好地服务客户。2019年,公司质量保证部完善了116个基于全球化发展和法规更新的SOP,为全球化项目合作提供体系支持,负责了15次海内外客户稽查,无重大问题;实施51次研究中心稽查,完成18个内部体系稽查,防范风险发生,优化业务流程。
2019年,公司临床运营部19个项目的25家中心接受国家局现场核查,全部顺利通过。
上述一系列举措,不仅给公司带来业绩增厚和业务能力的提升,也完善了全球跨区域的业务布局以及上下游产业链的进一步延伸。
2、与众多国内优秀的客户一同成长,更加坚定了公司要为中国创新药研发作出贡献的决心。公司非常有幸地见证了过去10多年来中国创新药发展的过程。中国的创新药也在这个期间从个别公司的孤军奋战到现在的万马奔腾,监管体制也在不断创新,并逐渐与全球接轨。中国作为一个人口大国,不可能只靠进口药品解决临床和患者需求,因此未来必须要依靠更多优秀的创新药企业,研发真正有临床价值的创新药。这个过程肯定会有很多曲折,但中国创新药产业还处于起步阶段,完全有能力在未来借助研究者、患者等方面的优势,以相对较小的成本,做出更好的产品,让中国新药走向世界舞台。2019年获批的13个中国1类新药中,7个由泰格医药或子公司助力研发。
2019年8月26日,由重庆永仁心医疗器械有限公司研发的植入式左心室辅助系统获批上市,该产品是我国首个获批上市的植入式心室辅助产品,填补了我国在人工心脏领域的产业空白。泰格捷通作为医疗器械领域领先的CRO,为重庆永仁心提供了全过程的临床试验服务。
2020年1月23日,泽璟制药在上海证券交易所科创板鸣锣上市。泽璟制药是一家专注于肿瘤、出血及血液疾病、肝胆疾病等多个治疗领域的创新驱动型新药研发企业。泰格医药在多个新药临床研究项目中同泽璟制药开展了深入合作。
2019年11月,由浙江同源康医药股份有限公司研发的1类靶向抗癌新药TY-302胶囊获临床试验默示许可,用于激素受体阳性和表皮生长因子受体2阴性(HR+/HER2-)局部晚期或转移性乳腺癌等晚期实体瘤或血液系统肿瘤的治疗。公司为其临床试验申报提供全过程服务。
3、积极参与国外创新药项目,为中国患者带来希望
2019年10月,由英国RSR公司研发的水通道蛋白抗体(AQP4Ab)检测试剂盒(酶联免疫法)获国家药监局批准上市。该试剂盒是国内首个获批临床上用于辅助诊断视神经脊髓炎(NMO)/视神经脊髓炎谱系疾病(NMOSD)的产品,将帮助更多NMO/NMOSD患者获得更为精准的诊疗。泰格捷通作为医疗器械领域领先的CRO,为该产品的获批提供了包括产品注册、临床研究等在内的全过程技术服务。
2019年11月,GSK宣布,其用于慢阻肺(COPD)稳定期治疗的长效三联吸入制剂“全再乐”(Trelegy Ellipta)获得中国国家药品监督管理局上市批准。这是首个在中国获批的每日一次三合一吸入制剂,泰格医药子公司思默医药为该药物临床研究提供了全过程的SMO服务(Site Management Organization,临床试验现场管理组织)。另外,Trelegy Ellipta也是全球首款获批的每日一次COPD三联闭合疗法,最早于2017年在美国上市。此次在中国获批,有望给中国的COPD患者带来新的希望。
4、坚持共赢,发展战略合作伙伴
2019年5月,公司及方达医药与浙江康恩贝(600572)制药股份有限公司(以下简称“康恩贝”)签署战略合作意向协议。本次签署战略合作协议,泰格医药、方达医药与康恩贝将充分发挥自身在医药产业链上的能力和优势,围绕以产品为核心展开合作。泰格医药和方达医药将为康恩贝提供药物一致性评价、新药临床研究、上市后药品临床再评价等相关服务,双方还将在打造新药孵化平台、股权投资、市场销售等方面开展深入合作。
2019年7月,公司与阿斯利康中国宣布达成战略合作,宣布双方将秉持“以患者为中心”的高度一致理念,在创新医药产品的临床研究和开发过程中进行全方位战略合作。阿斯利康作为一家以创新为驱动的全球综合型生物制药企业,近年来在支持和推动新药研发和商业模式创新方面有着卓越表现。
2019年8月,与韩国国家临床试验支持基金会(KoNECT)达成合作,推动中韩医药产业交流。双方的本次合作旨在推动中国和韩国新药开发和临床研究的合作和交流,并进一步提高新药临床研发成功率。为促进中国和韩国的医药产业发展和新药研发,双方将积极开展沟通和交流,扩大在中国和韩国的临床研究合作,分享新药研发相关经验。
2019年9月,宣布与无锡高新区达成合作,成为首家入驻无锡国际生命科学创新园企业,将为创新园中的创新医药公司提供临床研究全过程专业服务,加速医药研发,助力科技创新成果转化。无锡国际生命科学创新园由无锡高新区与全球知名生物制药企业阿斯利康共同打造,面向国内外创新公司,建设一个覆盖生命科学领域早期研发、创新孵化、成果转化、智能展示、专业服务为一体的孵化创新平台,构建医疗创新生态圈。
2019年9月,与深圳市坪山区人民政府达成合作,合作建设临床研究一体化服务平台。粤港澳大湾区是我国开放程度最高、经济活力最强的区域之一,在国家发展大局中具有重要战略地位。深圳作为粤港澳大湾区四大中心城市之一,在生物医药产业领域也将发挥尖兵作用。生物医药产业是深圳市坪山区的重点发展产业,以赛诺菲巴斯德、微芯生物为代表的大型企业和以普瑞金、华先医药等为代表的中小微创新型企业相互促进、共同发展的产业格局,具备全面提速发展的良好产业基础。泰格医药作为行业领先的临床研究CRO,也将充分发挥自身在临床研究全过程的专业服务能力,通过此次合作建设临床研究一体化服务平台,把握历史机遇,为更多粤港澳大湾区生物医药创新企业提供优质服务,助力粤港澳大湾区生物医药创新高地建设。
新形势下CRO与临床试验机构的战略共建合作模式。2019年6月,“2019中国临床试验机构创新实践高峰论坛”在北京举行,会上大家共同就临床研究中的机遇与挑战,如何落实国家医药改革创新政策,提升临床试验机构管理水平和临床研究质量,共同促进医药研发的进步与发展等话题进行了探讨。在新形势下,CRO与临床试验机构紧密合作,也可以考虑从单一的项目外包合作逐渐转变成长期的战略合作模式,尤其和规模化、规范化CRO,可以进行纵向+横向的全方位战略合作,实现协作共赢。
公司投资的颐柏健康是一家打造以临床试验研究中心为核心竞争力、围绕着为临床试验研究中心提供全方位服务为特色的医疗集团,在和临床试验机构战略共建方面拥有丰富的经验。希望CRO和临床试验机构在未来进一步加强合作与互动,形成更多全方位的长期紧密战略合作,优势互补、合作共赢,做好项目,助力中国新药研发。
三、风险
1、客户对生物制药研发服务的需求或开支下降可能对我们的业务、财务状况、经营业绩及前景产生重大不利影响。
2、行业政策风险。公司属于医药研发行业,受相关政策影响较大,监管机构可能会更改相关法律及监管规定。
3、服务质量风险。如果公司的服务无法达到客户标准或满足客户需求,会有流失客户或无法吸引客户的风险。客户或会将部分或全部业务转至公司的竞争对手,减少或终止与公司的业务合作,可能会对公司的声誉、业务、财务状况、经营业绩及前景造成不利影响。
4、人力资源风险。临床试验专业人才是公司发展的根本。在医药研发人才市场激烈竞争的情况下,经验丰富且专业能力强的人才炙手可热,公司必须提供具有竞争力的薪酬及福利计划以吸引及挽留人才。如果公司不能聘用或挽留足够数量的专业人员以保持公司预期增长和维持稳定的服务水平,可能会对公司的声誉、业务、财务状况、经营业绩及前景造成不利影响。
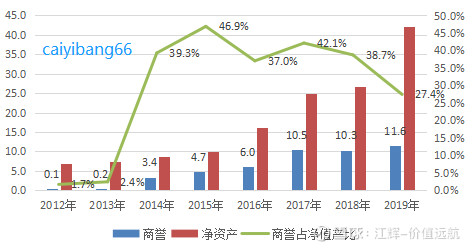
5、收购及业务整合风险、商誉及其他无形资产的减值风险
6、新型冠状病毒肺炎疫情的影响
公司业绩可能会受到新型冠状病毒肺炎疫情的影响。目前公司并没有出现因新型冠状病毒肺炎疫情被取消的项目,但医院为感染新型冠状病毒肺炎的患者投入大量医疗资源,导致用于临床试验的资源变少。同时,出于潜在感染的担忧,在新型冠状病毒疫情期间有患者不太愿意参与临床试验,这给公司的患者招募工作带来挑战。由于新型冠状病毒肺炎疫情继续演变并影响到全球各地,目前很难确定我们未来是否会遭遇客户订单减少及/或客户流失的情况,以及公司现有和未来的项目是否会因新型冠状病毒肺炎疫情而受到实质性干扰或延误。新型冠状病毒肺炎疫情可能继续对我们的业务、前景及经营业绩产生不利影响的程度,这些不确定性目前无法合理估计。
周末我会再出深度分析内容。
水晶球APP
高手云集的股票社区
X




 公安备案号 51010802001128号
公安备案号 51010802001128号