-
个股研究系列:中国创新药领军企业微芯生物
股市战友 / 2020-02-24 10:51 发布
一、前言
前两天把科创板的所有上市公司简单的翻看了一下,确实都是科技类创业型上市公司,只有部分能够在最近三年实现稳定盈利,不少公司的利润波动都很大。这些上市公司未来肯定会有一些成长为大公司,也会有不少公司生存艰难。投资其中的公司必须要研究透彻,而且现在的估值实在是太高,大部分都不适合。大致看了一下,半导体集成电路、5G、计算机软硬件等高科技相关企业占比较高,生物医药板块也有一些,不是特别多。
看完之后选了12家公司加入了观察名单,其中一半是生物医药器械板块的,其它都是计算机集成电路相关公司。计算机集成电路相关行业接触了一段时间,涉及的行业知识很多,暂时还没能力理解吸收,未来继续关注学习。生物医药器械板块看了一下,估值确实高,这跟科创板上市不久,资金关注高,加上去年科技股行情,估值就这么整体抬上来了。估值高可以不考虑介入,跟踪也是一件乐趣无穷的事情。
第一家深入跟踪的个股我们选择微芯生物,这是一家以创新药为主的上市公司,主要方向就是肿瘤、代谢性疾病、自身免疫性疾病的研究。
我们持续看好生物医药器械板块大家都应该很清楚,在去年集采出来以后我们给出的大方向就是跟创新有关的生物医药器械板块上市公司,微芯生物完全符合我们的要求,具体情况我们一起来了解一下。
二、所处行业基本面状况
医药行业作为国家战略新兴产业,深受国家政策影响,国家相关政策将继续推动医疗健康产业的快速发展。随着我国老龄化趋势提速、二胎政策放开、国民经济的发展、医疗卫生体系的完善及居民健康意识日益提升,人们对生物医药产品的需求逐渐增加,医药行业市场总量在逐年增长。国家关于“健康中国”等新的战略方针及对医药行业支持政策的出台与实施,更是给医药行业整体提供了新的发展契机,加快医药行业企业的发展。
随着世界经济的发展、人口总量的增长、社会老龄化程度的提高以及民众健康意识的不断增强,全球医药行业保持了数十年的高速增长。2019年全球药品市场需求将达12249亿美元,2015-2019年全球药品市场需求年均复合增长率将维持在4%-5%之间;新兴市场的药品需求增长尤其显著,亚洲(日本除外)、非洲、澳大利亚2014年至2019年的医药市场增速将达到6.9%-9.9%,超过同期预计全球4.8%的增速水平。
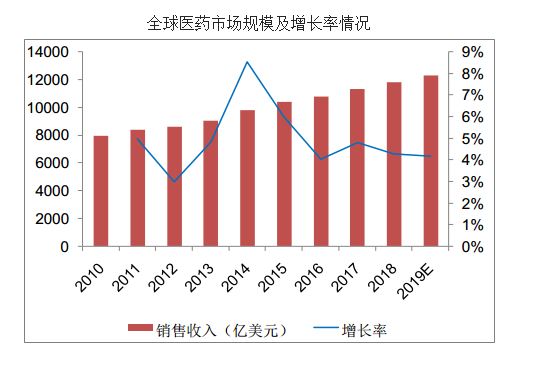
中国是医药行业全球最大的新兴市场,我国医药工业总产值从2007年的6719亿元增长到2017年的35699亿元,年复合增长率为18.2%。
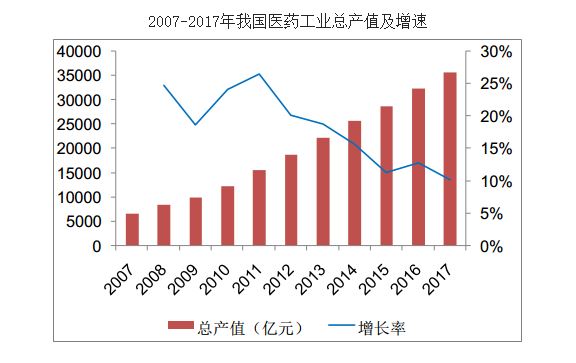
根据《全球药品市场展望2021》,2016 年全球医药费用主要用于治疗肿瘤(753 亿美元)、糖尿病(662 亿美元)、自身免疫类疾病(451 亿美元)、疼痛(670亿美元)、心血管疾病(705 亿美元)等。2016 年-2021 年,肿瘤的治疗费用将会是全球医药市场增长最快的领域,年复合增长率将达到9-12%,预计2021 年将达到1,200-1,300 亿美元。2016 年-2021 年,糖尿病将居于全球医药市场第二大领域,年复合增长率将达到8-11%,预计2021 年将达到950-1,100 亿美元规模。
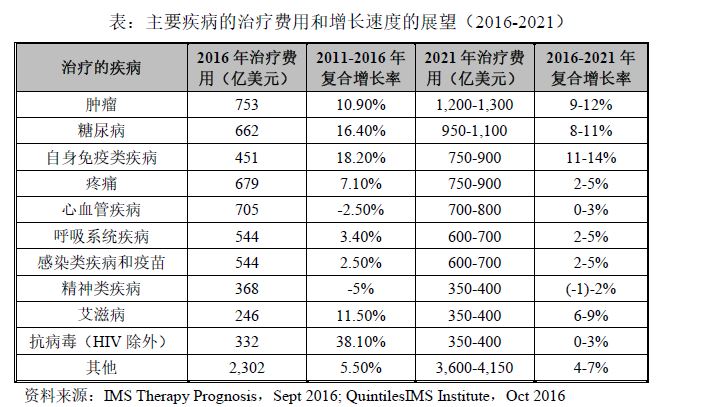
微芯生物聚焦肿瘤、代谢性疾病、自身免疫性疾病是未来增速最快的三个领域,也是市场规模最大的用药疾病,产品未来市场空间比较大。
三、公司简介
深圳微芯生物科技有限责任公司(简称微芯生物)是由资深留美归国团队所创立的生物高科技领先企业,专长于原创小分子药物研发。原创团队及本土团队在生物医学研究领域具有较高的科学造诣,有创新药研发和管理的实战经验,在欧美具有创建和管理企业的成功经历,熟知全球药品管理技术法规和专利策略,谙熟中国药品市场。公司始终秉承:“原创、安全、优效、中国——致力于为患者提供可承受的创新机制治疗药物。”
支持公司可持续发展的核心技术,是我们自主构建的基于化学基因组学的集成式药物创新与早期评价技术体系。本平台体系有效地整合了包括计算机辅助药物设计、药物及组合化学、高通量高内涵药物筛选、化学基因组学基因表达谱研究、生物信息学和化学信息学数据挖掘等多项现代技术,能有效加速小分子创新药物的研发历程、降低新药开发风险,是研发出具有临床差异化新药的重要技术,也是支撑微芯生物未来可持续发展的重要保障。
微芯生物根据国际新药研发的规律并结合中国医药市场现状,探索出了一条在保留中国产品经营权益的同时,对国际制药公司实施专利授权、建立国际临床联合开发而实现收益的企业发展之路;同时,针对性地建立与跨国制药企业高水准合作研究的商业模式。通过此发展策略,微芯生物在研创新药不仅可以尽快在中国上市销售,还能通过国际临床联合开发的模式,实现未来中国原创药进入全球市场销售的目标。这一创新发展模式——通过专利授权、合作研究和产品最终上市销售实现盈利和发展——改变了中国本土医药企业缺乏原创药这一实质性缺陷,开创了从“中国仿制”到“中国创制”的先河。
微芯生物自成立以来,围绕建立以专利和创新药物为核心竞争力的企业发展战略,在新药研发、知识产权、商务发展等方面均取得了突破性进展,已实现了多个行业领域的第一,为中国创新药物事业做出了积极贡献。作为自主创新与前沿平台技术集一身的中国创新药物公司,自成立以来便备受行业与媒体的关注与瞩目,先后被包括美国《商业周刊》、《时代周刊》、《自然生物技术》等多家杂志和媒体所报道。多次应邀在国际生物医药行业主要会议上围绕新药研发做主题演讲,为企业在国内、国际制药领域的影响力奠定了基础。
四、公司主要产品及主营业务收入情况
公司主要产品均为自主研究发现与开发的新分子实体且作用机制新颖的原创新药。目前,正式上市销售的只有一个产品,国家1 类原创新药西达本胺(商品名为“爱谱沙®/Epidaza®”),其是全球首个亚型选择性组蛋白去乙酰化酶(HDAC)抑制剂。主要针对第I类HDAC中的1、2、3亚型和第IIb类的10亚型, 具有对肿瘤异常表观遗传功能的调控作用。西达本胺通过抑制相关HDAC亚型以增加染色质组蛋白的乙酰化水平来引发染色质重塑,并由此产生针对多条 信号传递通路基因表达的改变(即表观遗传改变),进而抑制肿瘤细胞周期、诱导肿瘤细胞凋亡,同时对机体细胞免疫具有整体调节活性,诱导和增强 自然杀伤细胞(NK)和抗原特异性细胞毒T细胞(CTL)介导的肿瘤杀伤作用。西达本胺还通过表观遗传调控机制,具有诱导肿瘤干细胞分化、逆转肿瘤细胞的上皮间充质表型转化(EMT)等功能,进而在恢复耐药肿瘤细胞对药物的敏感性和抑制肿瘤转移、复发等方面发挥潜在作用。

2014年12月, 获国家食品药品监督管理总局(CFDA)批准上市。其首个适应症为复发及难治性的外周T细胞淋巴瘤。目前还有其它适应症处于新药上市申请和III期临床试验过程中,具体情况见下一章节在研项目。
1、 西达本胺的营业收入情况
目前,公司主营业务收入主要来自于西达本胺片在国内的销售收入和西达本胺相关专利技术授权许可收入。招股说明书显示,公司主营业务收入快速增长。2016年度、2017 年度及2018 年度,公司主营业务收入分别为8,535.09 万元、11,050.34万元及14,768.90 万元,年均复合增长率为31.54%。
公司主营业务收入的构成情况如下:
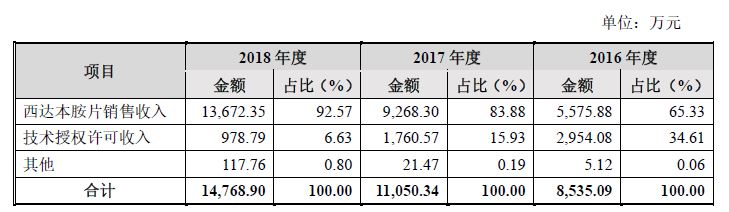
2、 西达本胺治疗外周T 细胞淋巴瘤(PTCL)优势
西达本胺片的上市填补了我国治疗外周T 细胞淋巴瘤药物的空白。上市以来,西达本胺得到了广大医生、专家和患者的认可,已广泛应用于外周T 细胞淋巴瘤(PTCL)的临床治疗。2016 年4 月《中国肿瘤临床》杂志刊登了由中国临床肿瘤学会(CSCO)、中国抗淋巴瘤联盟(UCLI)、中华医学会血液学分会(CSH)白血病·淋巴瘤学组、中国抗癌协会血液肿瘤专业委员会及中国抗癌协会淋巴瘤专业委员会发布的《西达本胺治疗PTCL 的中国专家共识(2016 版)》,一致认可西达本胺对外周T 细胞淋巴瘤良好的治疗作用,认为西达本胺是中国外周T 细胞淋巴瘤患者的二线首选药物。
如下表所示,与其他PTCL 治疗方案相比,西达本胺具有较大的优势。
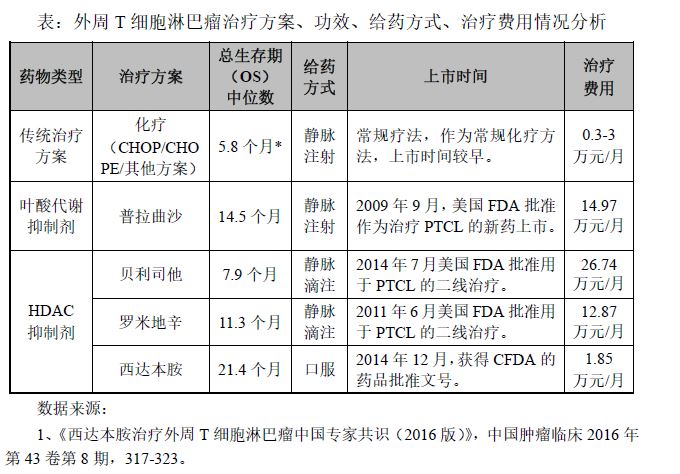
使用西达本胺的PTCL 患者的总生存期更长,明显优于治疗外周T 细胞淋巴瘤的其他二线方案(普拉曲沙、罗米地辛和贝利司他)。西达本胺为口服制剂,依从性好,且1 周2 次服药即可。对不宜静脉治疗、不适合住院治疗的老年患者,西达本胺为唯一的治疗选择。
公司充分考虑中国患者的支付能力,西达本胺的上市定价较低。国际同类药物中,贝利司他治疗费用26.74 万元/月、罗米地辛治疗费用12.87 万元/月,而西达本胺于2017 年7 月进入国家医保目录(2017 年版)后,零售价格统一调整为385 元/片(5mg/片),治疗费用降至1.85 万元/月,考虑各地区医保报销比例45%-90%,患者承担费用远远低于国外同种药品的治疗费用,进一步减轻了患者使用西达本胺的经济负担。大大提高了药品的可及性,使更多的外周T 细胞淋巴瘤(PTCL)患者在疗效和支付能力方面受益于西达本胺这一原创新药。
3、 外周T 细胞淋巴瘤(PTCL)适应症的市场空间
由于外周T 细胞淋巴瘤为罕见病,目前尚无第三方发布的市场容量和市场占有率研究数据。西达本胺(PTCL)的适应症为复发或难治的外周T 细胞淋巴瘤,针对此类适应症患者,国内目前批准的治疗药物仅为西达本胺,没有竞争药物。公司估算西达本胺(PTCL)目前的临床使用率情况如下:2018 年度公司西达本胺片的使用量(包含销售、后续免费用药和慈善捐助)为2.57 万盒,西达本胺片的用药频率为2 盒/月,按最大用药量24 盒/年计算,2018 年度使用西达本胺片的患者人数约1,071 人。因此,根据外周T 细胞淋巴瘤患者人数和西达本胺片用药人数,估算出西达本胺片目前的临床使用率约为7.44%。
公司结合权威机构关于外周T 细胞淋巴瘤的统计数据以及自身关于西达本胺临床使用率及销售价格的估计,对西达本胺(PTCL)达到销售峰值时的理论使用量和理论市场规模预测如下:PTCL 患者每年新增人数约1.44 万人;西达本胺片已于2017 年纳入国家医保目录,且对于复发或难治的外周T 细胞淋巴瘤患者,西达本胺被推荐为首选药物,目前亦为唯一药物;公司管理层基于西达本胺认知度提升和未来可能出现的竞争药品等情况,预估外周T 细胞淋巴瘤患者中约30%会使用西达本胺治疗;考虑到西达本胺新增适应症、医保谈判及未来可能出现的竞争药品等情况,预估西达本胺片达到理论使用量时的销售价格约为5,880 元/盒;西达本胺片用药频率为2 盒/月,即每个PTCL 患者用药为24 盒/年。因此,西达本胺(PTCL)的理论使用量为10.37 万盒/年,理论市场规模为6.10 亿元/年。按目前公司的销售额,未来还有很大增长空间。
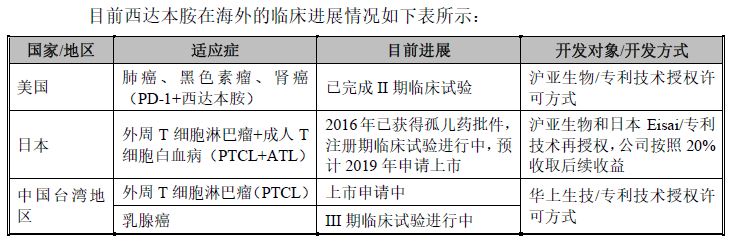
4、 西达本胺专利权的海外技术授权许可
2006 年10 月,公司通过“许可费+里程碑收入+收益分成”的技术授权许可方式将西达本胺在美国、日本、欧盟等国家或地区的权利授权给沪亚生物国际有限责任公司(美国企业);由其在美国、日本、欧盟等地进行海外开发与商业化,实现中国原创新药的全球同步开发、参与全球市场竞争的目标。公司与沪亚之间的合作,使西达本胺成为中国首个授权美国等发达国家使用境外发明专利以实现全球同步开发与商业化、并获得技术授权许可收入的原创新药,开创了中国创新药对欧美进行专利授权(License-out)的先河。
2013 年9 月,公司将西达本胺在中国台湾地区的权利授权给华上生技医药股份有限公司(台湾企业),由其在中国台湾地区进行开发与商业化。
五、微芯生物的研发情况
1、 研发投入
公司作为创新型生物医药企业,一贯将创新与研发视为核心竞争力。截至2018 年末,公司研发人员共104 名,占员工总数的28.03%,包括3 位国家级领军人才和2 位海外高层次人才,累计获得8 项家“重大新药创制”重大科技专项、7 项国家高技术研究发展(863)计划、1 项国家科技型中小企业技术创新基金、1 项中国科学院战略性先导科技专项、1 项“国家重点研发计划”重点专项、5 项广东省科技计划和17 项深圳市科技计划资金资助。2016 年、2017 年、2018 年,公司研发投入占营业收入的比例分别为60.52%、62.01%和55.85%。
公司针对新药研发周期长、投入高、风险大的特点,围绕公司产品链在化合物通式、制备方法、晶型、剂型和用途等方面,运用专利保护策略在境内外实施了全链条、全生命周期的专利布局,不断加固专利保护壁垒、延伸专利保护期限。
截至招股说明书签署日,公司累计申请境内外发明专利百余项,已获得59 项境内外发明专利授权(其中境外发明专利授权42 项)。公司已获准上市的抗肿瘤药物西达本胺的化合物中国发明专利于2017 年获得国家知识产权局和世界知识产权组织联合颁发的“中国专利金奖”。公司已上市产品西达本胺也是中国首个授权美国等发达国家使用境外发明专利以实现全球同步开发与商业化、并获得技术授权许可收入的原创新药,开创了中国创新药对欧美进行专利授权(License-out)的先河。
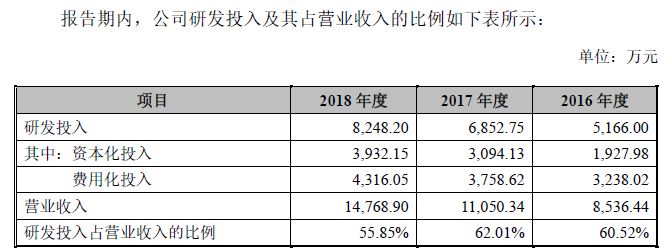
从研发投入资金和研发人数占比来看,公司是非常重视研发的,这为后期储备了一些很不错的项目。
2、 公司在研项目申请的情况(截止2018年底)

3、 在研项目西达本胺用于激素受体阳性晚期乳腺癌适应症的具体情况
西达本胺治用于激素受体阳性晚期乳腺癌适应症,于2018年11月2日,深圳微芯生物科技股份有限公司、深圳微芯药业有限责任公司递交的本药品注册申请获受理(受理号:CXHS1800033 国)并列入优先评审。并于2019年11月30日获批增加适应症:“联合芳香化酶抑制剂用于激素受体阳性、人表皮生长因子受体-2 阴性、绝经后、经内分泌治疗复发或进展的局部晚期或转移性乳腺癌患者”。
乳腺癌是发生在乳腺腺上皮组织的恶性肿瘤。乳腺癌中99%发生在女性,男性仅占1%。根据国家癌症中心发布的全国癌症统计数据,乳腺癌属于我国女性发病率最高的癌症,2014 年我国女性乳腺癌发病率41.82 人/10 万。在每年新发乳腺癌病例中3%~10%的妇女在确诊时即有远处转移,早期患者中30%~40%可发展为晚期乳腺癌。晚期乳腺癌患者的总体中位生存期为2~3 年,不同分子亚型的情况不同。其中激素受体(ER)阳性乳腺癌约占全部乳腺癌的70%,属于乳腺癌中比例最高的类型。根据米内网数据,2016 年我国乳腺癌用药总体规模已超过320 亿元,同比增长11.67%。据此估算2016 年我国激素受体阳性晚期乳腺癌用药总体规模约78.4 亿元。
临床应用中,针对晚期激素受体阳性乳腺癌患者主要采用不同机制药物联合用药的方式,并且在患者对某一类别药物产生耐药后会采用另一类别药物进行治疗。医生可能会选择不同的联合用药治疗方案,已上市的氟维司群和帕博西尼以及尚在临床阶段的其他机制药物获批上市后,可能会与西达本胺构成竞争关系,但亦有可能通过联合用药或在一类药物产生耐药性后进行替换用药,从而构成互补关系。另外,乳腺癌适应症的市场规模较大,相较已上市竞争药品,西达本胺作用机制新颖,在联合治疗中,除具备HDAC抑制剂特有的表观遗传调控特征外,还可通过调控乳腺癌细胞激素受体依赖和非依赖通路,发挥乳腺癌治疗作用,上市后将通过学术推广等方式及良好的疗效争取获得更多医生和患者的接受和认可。
公司肿瘤产品事业部市场总监负责西达本胺产品线,并已针对乳腺癌适应症招聘了1 名产品经理和1 名市场助理,主要负责产品市场定位、学术推广策略及方案制定。另外,公司已招聘18 名销售人员,主要负责产品市场调研等工作。公司计划在产品上市前继续招聘约15 名销售人员,在产品上市后第二年,视情况进一步招聘相关销售人员。
4、 在研项目西达本胺用于晚期非小细胞肺癌适应症的具体情况
非小细胞肺癌是除小细胞肺癌外所有肺癌组织分型的总称,包括鳞状细胞癌、腺癌和大细胞癌。根据国家癌症中心发布的统计数据,2015 年我国新发肺癌病例78.7 万人,经过年龄标准化的肺癌年发病率约为35.96/10 万人。非小细胞肺癌约占总体肺癌患者的85%,据此推算2015 年我国新发非小细胞肺癌病例66.90 万人,经过年龄标准化的年发病率约30.57/10 万人。
针对晚期非小细胞肺癌,如果存在驱动基因(EGFR、ALK、ROS)突变,临床指南推荐选用特定靶向治疗药物。西达本胺的主要竞争药物为其它没有明确驱动基因突变的晚期非小细胞肺癌患者的治疗药物。在过去的临床治疗中,此类患者首选化疗药物组合,VEGF 抑制剂贝伐珠单抗可以联合化疗作为一线治疗方案。2018 年以来,国内批准了2 款PD-1 抗体药物帕博利珠单抗、纳武单抗以及1 个小分子VEGF 抑制剂安罗替尼,分别用于一线联合用药治疗、二线单药治疗和三线单药治疗,其它PD-1 或PD-L1 抗体和小分子VEGF 抑制剂也处于不同的临床研究阶段。
西达本胺用于晚期非小细胞肺癌适应症,目前III期临床试验正在进行中。北京大学肿瘤医院朱军教授在关于西达本胺在PTCL中取得的最新研究进展。该研究共纳入既往均接受过1次以上的全身治疗(包括化疗、造血干细胞移植),但无缓解或缓解后复发的1279例PTCL患者,其中725例(52%)患者接受西达本胺单药治疗、另554例(43%)患者接受西达本胺联合化疗,联合治疗方案共有三种:西达本胺+CHOP或类CHOP方案(181例)、西达本胺+铂类方案(157例)以及西达本胺+其它方案(216例)。其研究终点指标主要包括:完全缓解率(CR)、客观缓解率(ORR)以及临床获益率(DOR)。该研究的治疗人群涵盖了PTCL的各种亚型,包括:外周T细胞淋巴瘤,非特指型(PTCL-NOS)、血管免疫母细胞性T细胞淋巴瘤(AITL)、间变大细胞性淋巴瘤(ALCL)、结外NK/T细胞淋巴瘤(NKTCL)等。
研究结果表明,对于PTCL患者而言,西达本胺的单药及联合治疗均有较明显的疗效。整体上,西达本胺联合治疗的疗效优于单药治疗,其CR率分别为19% (单药)vs 20%(联合);ORR分别为48%(单药)vs 66%(联合);DOR分别为71%(单药)vs 82%(联合)。三种联合方案的数据显示:西达本胺+CHOP/类CHOP方案的CR为20%、ORR为71%、DOR为86%;西达本胺+铂类的CR、ORR以及DOR依次为13%、64%以及77%;其它联合方案的CR、ORR以及DOR依次为25%、63%和83%。三种联合方案的ORR并无显著差异。
5、 在研项目西格列他钠用于2 型糖尿病的适应症的具体情况
国家1类新药西格列他钠是公司自主设计、合成、筛选和开发的新一代胰岛素增敏剂类新分子实体,针对2型糖尿病现已完成III期临床试验,也是全球最早完成III期临床试验的 PPAR 全激动剂。可以持续控制血糖及伴随脂代谢紊乱的严重胰岛素抵抗和糖尿病。公司已经提交新药上市申请,并于2019 年 9 月 19 日收到国家药品监督管理局下发的抗 II 型糖尿病国家 1 类新药西格列他钠片新药上市申请(NDA)的 《受理通知书》。未来关注审批进度,一旦上市,可以进一步丰富公司产品线,我们估计最快2021年有上市的可能。
2 型糖尿病治疗药物主要包括胰岛素制剂、双胍类、糖苷酶抑制剂类、磺酰脲类、胰高血糖素肽-1(GLP-1)类似物、二肽基肽酶-4(DPP4)抑制剂、噻唑烷二酮(TZD)类。根据米内网数据,2016 年我国糖尿病医院用药规模为397 亿元,同比增长 8.77%。2 型糖尿病药物治疗的首选是二甲双胍。不适合二甲双胍治疗者,可选择口服 α-糖苷酶抑制剂或胰岛素促泌剂。单独使用二甲双胍治疗而血糖仍未达标,可加口服胰岛素促泌剂、α-糖苷酶抑制剂等药物,或者口服二甲双胍加注射胰岛素等药物。预计公司产品西格列他钠未来上市销售后,将进入二联治疗方法,与二甲双弧联合用于 2 型糖尿病的治疗。
六、微芯生物本次募集资金投向
本次公司公开发行5,000 万股人民币普通股,发行价30.43 元,发行市盈率467.51 倍,募集资金总额102,150.00万元。将根据轻重缓急依次投资于以下项目:
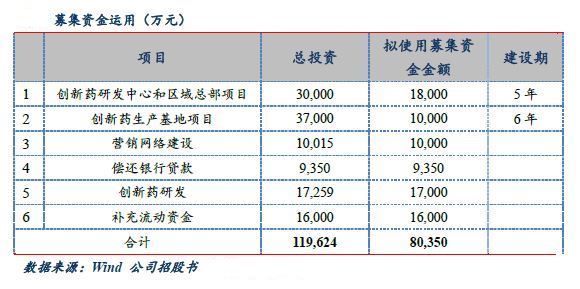
创新药研发中心和区域总部项目建设周期5 年,预计 2020 年末正式投入使用。
创新药生产基地项目包括非肿瘤创新药生产及辅助设施(一期)、肿瘤创新药生产及辅助设施(二期),为原创抗 2 型糖尿病新药西格列他钠和原创抗肿瘤新药西奥罗尼在成都市高新西部园区配套建设符合美国、欧盟cGMP 标准和中国 GMP 标准的小分子药物生产基地。建设规模西格列他钠原料药1.7t,片剂10500 万片,西奥罗尼0.4t/a,胶囊2000 万粒。项目建设周期计划为6 年,分两期建设,预计于 2020 年完成建设。投资总额为 37,000 万元,项目建成后,预计税后内部收益率为27.10%,经济效益良好。
创新药研发项目主要用于以下项目的研发和推进:
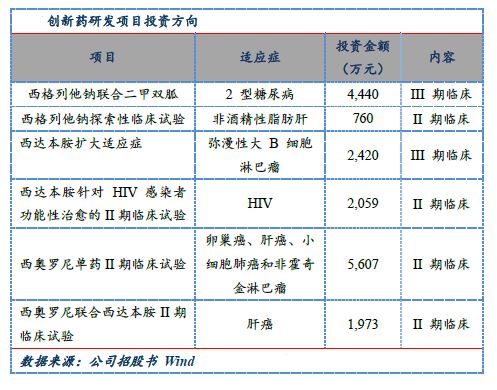
从公司披露的募集资金投放项目,我们可以清楚的看到在为即将上市的西达本胺新适应症和西格列他钠上市做准备,后续继续跟踪其它项目的进展情况。
七、微芯生物的主要财务数据
微芯生物刚刚上市不久,可查数据并不多,目前只有最近三年的数据。2017年净利润同比涨幅最快,超过3倍,2018年回落到30%左右,2019年三季度净利润同比增速回落到38%附近。公司营业收入增长一直保持在30%-40%之间,增长相对稳定。因为数据相对较少,参考价值并不高。
2016年以来的具体数据见下表
科目\年度
2019-9
2018
2017
2016
2015
2014
基本每股收益(元)
0.0866
0.0690
0.0159
净利润(元)
3116.48万
2407.39万
524.43万
净利润同比增长率
29.45%
359.05%
营业总收入(元)
1.48亿
1.11亿
8536.44万
营业总收入同比增长率
33.65%
29.45%
每股净资产(元)
1.32
1.25
0.59
净资产收益率
6.70%
9.23%
3.46%
1、 营业收入及增速
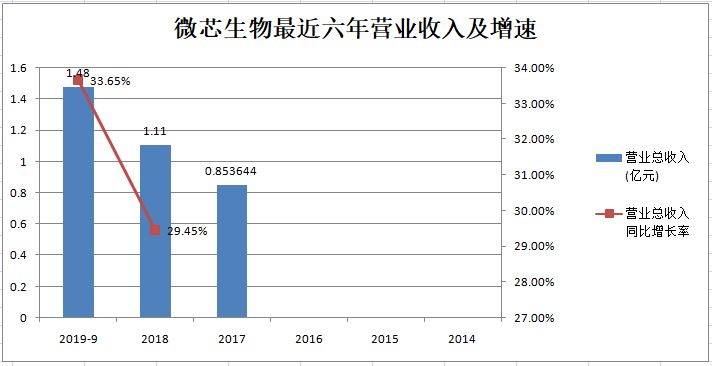
微芯生物最近三年的营业收入增长还算稳定,不过对于上市近5年的药品,这个收入并不高,这也说明目前这个适应症的市场空间不大。在2018年纳入医保的情况下,这个增速并不理想。接下去关注新适应症获批之后的推广效果,以及其它药品销售收入增长情况。
2、 净利润及增速
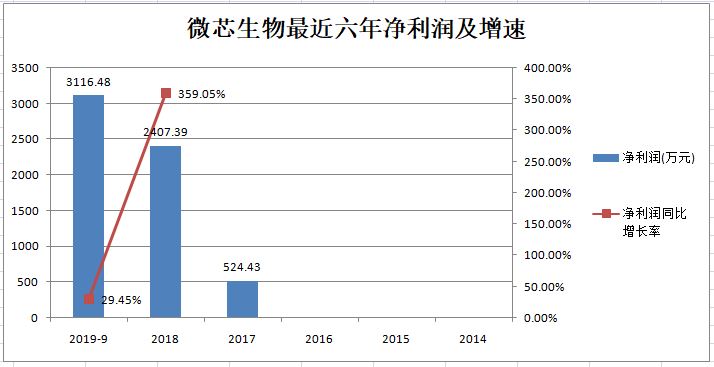
公司净利润增速波动很大,这个估计跟研发投入有关系。毕竟公司营业收入本来不高,研发投入又大。最重要的还是关注营业收入的增长。
八、股东情况研究
目前股东数在1.8-2万户之间,新股上市各机构配售获得的股份,参考意义不大,这里就不说了。
需要关注的是上市前公司股权结构,具体如下图:
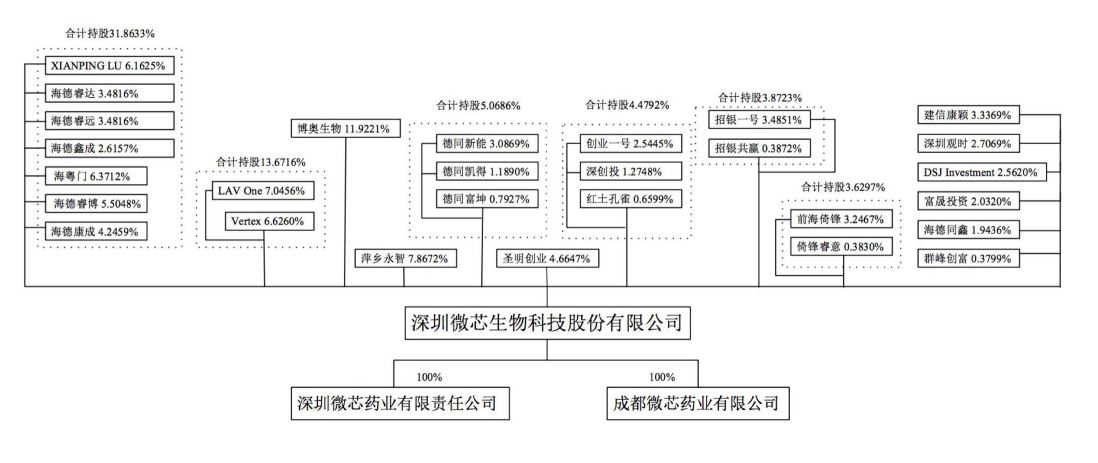
从中可以看到,不少产业资金、私募股权资金持股比例不少,这些资金在前期大量投入,科创板上市的目的肯定是要逐渐退出的,所以未来一旦解禁,股价的压力会非常大。从这个角度看,未来压制公司股价的一个重要因素,2020年8月份有超过50%的股份解禁,这个大小非的减持压力非常大,特别是估值比较高的情况下。对于新股我们一直坚持的就是三年之内要注意,两年之内坚决不碰。两年之后如果有大幅下跌到估值合理的位置,可以逐渐考虑。
九、技术面及估值分析
1、 中长期技术面分析
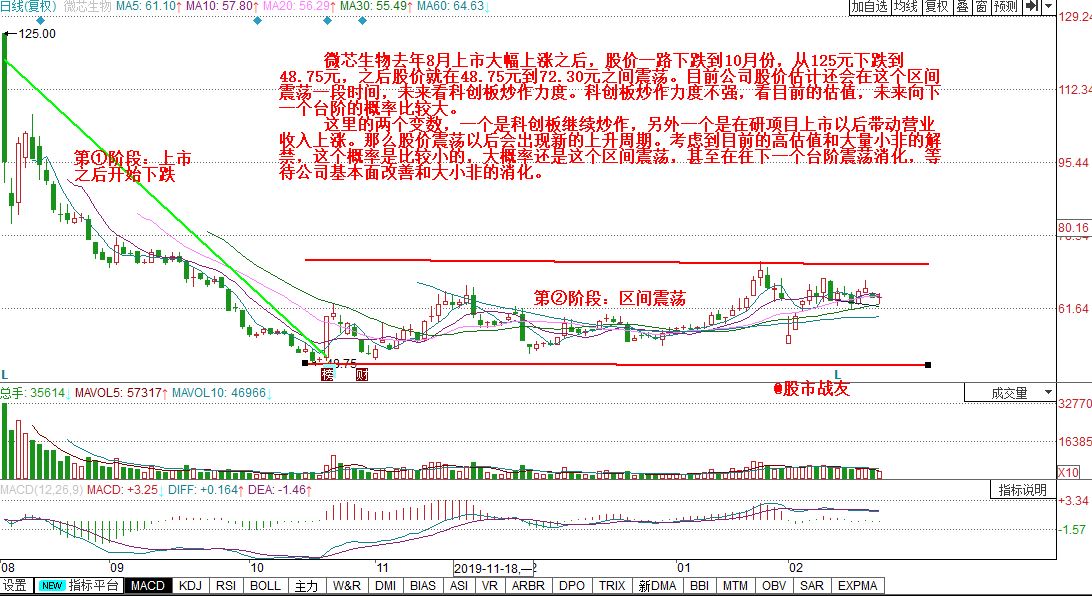
微芯生物去年8月上市大幅上涨之后,股价一路下跌到10月份,从125元下跌到48.75元,之后股价就在48.75元到72.30元之间震荡。目前公司股价估计还会在这个区间震荡一段时间,未来看科创板炒作力度。科创板炒作力度不强,看目前的估值,未来向下一个台阶的概率比较大。
这里的两个变数,一个是科创板继续炒作,另外一个是在研项目上市以后带动营业收入上涨。那么股价震荡以后会出现新的上升周期。考虑到目前的高估值和大量小非的解禁,这个概率是比较小的,大概率还是这个区间震荡,甚至在往下一个台阶震荡消化,等待公司基本面改善和大小非的消化。
2、 中短期技术面分析
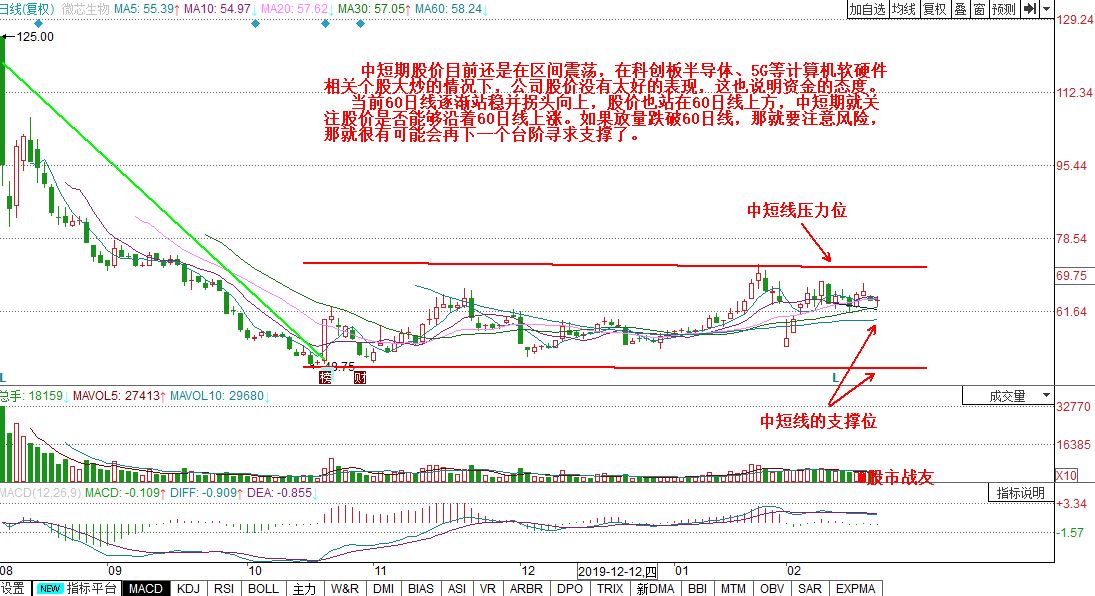
中短期股价目前还是在区间震荡,在科创板半导体、5G等计算机软硬件相关个股大炒的情况下,公司股价没有太好的表现,这也说明资金的态度。
当前60日线逐渐站稳并拐头向上,股价也站在60日线上方,中短期就关注股价是否能够沿着60日线上涨。如果放量跌破60日线,那就要注意风险,那就很有可能会再下一个台阶寻求支撑了。
3、 估值分析
对于个股的估值其实是很难说,毕竟涉及的影响因素太多,而且随时都会有变化,需要不断地修正。就目前来说,科创板股票没有一个估值是不高的,这跟目前的市场情绪有关系,未来5-10年都会是科技股的大时代。科创板在这个时候出现是有它的历史意义的,所以初期一定会是高估值。
现在整个科创板上市公司不多,资金也是源源不断的进来(科创基金的发售),所以整体估值都很高。目前就是一个市场情绪在发挥作用,未来是否会进一步抬高估值不好说,但是从长期价值投资角度来说并不是很好的时机。
从市盈率的情况来看,公司全年估计能够保持30%以上的增长,那么现在微芯生物的市盈率在900多倍,高不高。但是创新药企这个估值很难说,毕竟像泽璟制药亏损上市。这一类企业的投资就是高风险、高收益,未来能否带来股价的上涨,关键还是在研项目是否能够顺利推进上市,并且能够带动销售收入的上涨。目前来看,公司已上市品种销售收入增长一般,后续新适应症和新产品销售推广如何还不得而知。
以同类型上市公司贝达药业比较来说,也可以看出公司目前的估值确实高。不管是在研项目数量和上市市场空间,还是已上市品种的销售情况,以及市盈率,总市值等等,微芯生物都没有优势。如果不是2月20日贝达药业股价涨停,两者市值相差并不多。具体的比较就不做了,贝达药业具体的情况我们也是分析的很详细,可以去翻出来看看。
十、最后总结
1、 看好公司的创新药研发体系。公司专注于原创新分子实体药物的研发和生产,具备完整的从药物作用靶点发现与确证、先导分子的发现与评价到新药临床开发、产业化、学术推广及销售能力的国家级高新技术企业。已上市产品西达本胺是中国首个获得对规范市场技术授权许可收入的原创新药,是全球首个亚型选择性组蛋白去乙酰化酶(HDAC)抑制剂,用于PTCL 的治疗。
2、 公司开创了中国创新药对欧美进行专利授权(License-out)的先河,这也再次证明公司创新药的技术优势,海外市场一旦上市销售,公司将获得收益分成。2006 年10 月,公司通过“许可费+里程碑收入+收益分成”的技术授权许可方式将西达本胺在美国、日本、欧盟等国家或地区的权利授权给沪亚生物国际有限责任公司(美国企业);2013 年9 月,公司将西达本胺在中国台湾地区的权利授权给华上生技医药股份有限公司(台湾企业),由其在中国台湾地区进行开发与商业化。
3、 看好公司已上市品种西达本胺乳腺癌适应症获批之后,带动销量的增长。2019年11 月29 日,西达本胺获批增加适应症:联合芳香化酶抑制剂用于ER+、HER-2 阴性、绝经后、经内分泌治疗复发或进展的局部晚期或转移性乳腺癌患者。乳腺癌适应症的市场空间很大,而西达本胺的效果不错,为患者提供了新的治疗选择。在前期的乳腺癌耐药机制研究中,西达本胺展示出可以改善耐药并增敏已有治疗药物的作用。临床试验显示西达本胺联合依西美坦与单用依西美坦相比,可显著延长患者的无进展生存期(PFS),其中在有内脏转移的患者中差异更明显。同时,在客观缓解率、临床获益率方面均优于安慰剂联合依西美坦。
4、 看好公司已上市品种西达本胺非小细胞肺癌适应症获批之后,带动销量的增长。目前公司已经提交上市申请,预计在2021年前后获批。非小细胞肺癌适应症的市场空间也很大,不过竞争比较激烈。针对晚期非小细胞肺癌,如果存在驱动基因(EGFR、ALK、ROS)突变,临床指南推荐选用特定靶向治疗药物。西达本胺的主要竞争药物为其它没有明确驱动基因突变的晚期非小细胞肺癌患者的治疗药物。过去此类患者首选化疗药物组合,VEGF 抑制剂贝伐珠单抗可以联合化疗作为一线治疗方案。2018 年以来,国内批准了2 款 PD-1 抗体药物帕博利珠单抗、纳武单抗以及1 个小分子VEGF 抑制剂安罗替尼,分别用于一线联合用药治疗、二线单药治疗和三线单药治疗,其它 PD-1 或PD-L1 抗体和小分子VEGF 抑制剂也处于不同的临床研究阶段。
5、 看好公司在研项目西格列他钠未来的研发进展。1 类新药西格列他钠是新一代胰岛素增敏剂类新分子实体,现已完成 III 期临床试验,也是全球最早完成 III 期临床试验的PPAR 全激动剂,可以控制血糖,还可以治疗糖尿病患者具有的脂代谢紊乱。
6、 关注公司在研项目西奥罗尼的研发进展。小分子抗肿瘤原创新药西奥罗尼是一个多靶点多通路选择性激酶抑制剂,针对主要几种肿瘤相关靶标蛋白激酶 VEGFR1,2,3、PDGFRα/β、CSF-1R 和 Aurora B 均有显著的体外抑制活性,目前正在针对卵巢癌、小细胞肺癌、非霍奇金淋巴瘤、肝癌等不同适应症进行II 期临床试验。西奥罗尼的作用机制包括:抑制与血管生成相关的 VEGFR 和PDGFR,从而抑制肿瘤的新生血管形成,减少肿瘤的血液供应和生长;通过抑制细胞周期调控激酶Aurora B,从而抑制肿瘤细胞的周期进程,降低肿瘤的增殖活性;通过抑制与免疫细胞增殖活化相关的 CSF1R,从而抑制肿瘤局部免疫抑制性细胞的生长,提高机体对肿瘤的免疫监测和免疫清除功能。
7、 看好公司持续的创新投入,未来会收获不错的效果,而且公司的创新能力和创新效率是比较高的。公司研发投入占营业收入比重非常大,在所有上市公司里面排名靠前,2016 年、2017 年、2018 年,公司研发投入占营业收入的比例分别为60.52%、62.01%和55.85%。因为公司营业收入不大,所以投入金额并不算多,但是从上市和在研项目看,研发资金的使用效率和创新能力非常高。
8、 公司在科创板上市,目前的估值非常高,加上接下来面临大小非减持的压力,所以中长线投资的角度,短期都不会有非常好的介入机会。
9、 中短线投机的角度看,可以在目前震荡区间48-72元之间波段操作,但还是要注意在研项目和市场推广长时间不及预期,股价再下一个台阶震荡的风险。
10、总体上,我们看好公司创新药的研发,公司产品和在研项目几乎都是一类创新药物。目前还处于前期转化时期,所以相对来说风险也会比较大。一旦研发项目和市场推广不及预期,股价压力会比较大。考虑到目前的估值水平,结论就是可以长期跟踪公司基本面,未来一旦有明显改善,或者估值调整到合理区间,再考虑分批建仓布局。
以上内容还有很多不足之处,还望大家多指点指点,一起讨论,争取更加深入的了解公司情况。如果朋友有什么更好的信息和观点,我们可以继续探讨。
(整篇完结,谢谢转发!)
水晶球APP
高手云集的股票社区
X




 公安备案号 51010802001128号
公安备案号 51010802001128号